破解胃癌治疗“响应差异”之谜!中山大学肿瘤防治中心袁庶强教授&徐瑞华院士团队首次系统描绘胃癌新辅助免疫联合化疗疗效差异的完整图谱
| 导读 | 同时,关于APOA1+肿瘤细胞与TREM2+巨噬细胞轴线的发现,为开发逆转耐药的新型联合疗法指明了充满希望的方向。 |
近日,中山大学肿瘤防治中心袁庶强教授&徐瑞华院士团队在国际知名期刊《Cancer Cell》发表一项重磅研究,为胃癌的精准治疗带来了突破性进展。该研究首次系统描绘了胃癌新辅助免疫联合化疗(nICT)疗效差异的完整图谱,不仅揭示了导致治疗抵抗的关键细胞“对话”,还提供了可用于临床的精准分层工具。
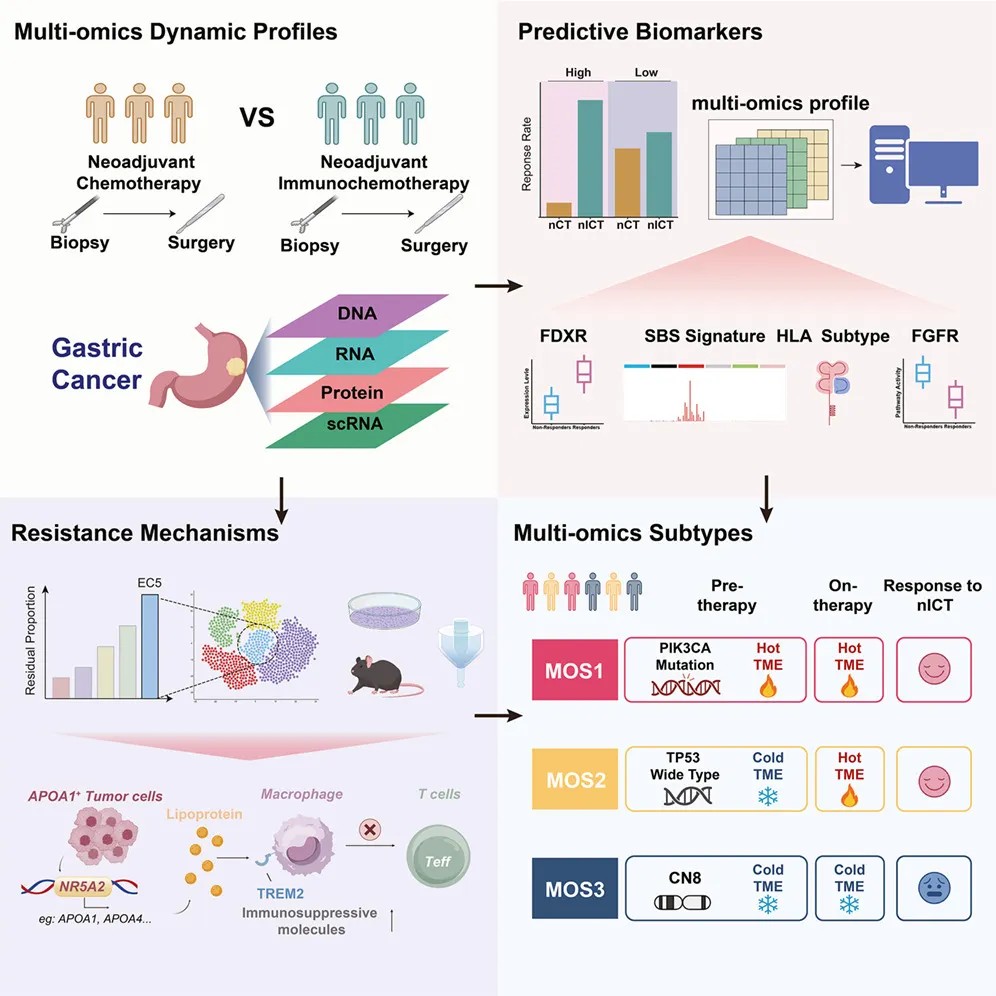
图形摘要
研究背景:机遇与挑战并存的胃癌新疗法
对于局部晚期胃癌患者,在手术前进行新辅助治疗以缩小肿瘤、提高手术成功率至关重要。近年来,免疫联合化疗(nICT)作为一种前景广阔的新策略,已显示出优于传统单纯化疗(nCT)的疗效。然而,并非所有患者都能从中同等获益,部分患者面临原发性耐药。如何提前甄别优势人群、并破解耐药机制,成为临床亟待解决的核心难题。
深度解析:五幅不同的肿瘤“微环境画像”
为了解答这一问题,研究人员对参与临床试验的110例胃癌患者样本进行了前所未有的多组学深度分析,涵盖了治疗前和治疗后的肿瘤组织。
研究最关键的发现之一,是依据肿瘤微环境的特征,将胃癌划分为五种截然不同的生态型(EC1-EC5):
-
EC1(T细胞激活型)、EC2(三级淋巴结构型)、EC3(血管正常化型):这三种类型的肿瘤微环境对nICT治疗更为敏感,是实现病理显著缓解的优势群体。
-
EC4(细胞外基质组织型)与EC5(免疫抑制巨噬细胞富集型):这两种类型则对nICT反应不佳,构成了治疗抵抗的主力军。其中,EC5型特征为富含具有免疫抑制功能的巨噬细胞,是典型的免疫“冷”肿瘤。
机制解析:癌细胞如何策反免疫细胞?
研究更进一步,精准锁定了EC5型肿瘤耐药的罪魁祸首。团队发现,这类肿瘤中有一群特殊的APOA1+肿瘤细胞,它们会主动与微环境中的TREM2+巨噬细胞进行“对话”。这种细胞间的相互作用,直接重塑并强化了免疫抑制微环境,导致免疫治疗失效,这一发现为逆转耐药提供了明确的靶点。
临床转化:从生物标志物到精准分层模型
除了揭示机制,研究的另一大价值在于提供了可直接指导临床实践的预测工具。团队鉴定出多个与nICT疗效密切相关的生物标志物:
-
基因层面:特定突变特征(SBS19)、HLA-B15:02*基因型。
-
表达层面:肿瘤细胞内FDXR基因的高表达。
-
通路层面:FGFR信号通路的活性。
最终,研究人员成功整合了基因组、转录组、病理图像等多维度信息,构建出一个强大的多组学分层模型。该模型能够准确地在治疗前预测患者所属的生态型及治疗反应概率,为实现“因人施治”的精准医疗奠定了坚实基础。
研究意义与未来展望
该研究不仅深入阐释了胃癌免疫化疗响应异质性的复杂生物学原理,更重要的是搭建了从基础发现到临床应用的桥梁。它提供的“五种生态型”分类框架和“多组学预测模型”,有望在未来帮助临床医生为每位胃癌患者选择最可能受益的治疗方案,避免无效治疗带来的副作用和经济负担。同时,关于APOA1+肿瘤细胞与TREM2+巨噬细胞轴线的发现,为开发逆转耐药的新型联合疗法指明了充满希望的方向。(转化医学网360zhyx.com)
原文链接:
https://www.cell.com/cancer-cell/abstract/S1535-6108(26)00054-1
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发