【Cell】颠覆认知!线粒体融合介导氧化磷酸化,促使癌细胞永生化!
| 导读 | 癌症是全球第二大死亡原因,仅在2018年就夺走了960万人的生命。癌症的发展极其复杂,且受多种因素相互作用的影响。直到最近人们才发现,大多数癌症,例如宫颈癌、胃肠道癌和乳腺癌等,都源自成体干细胞失控。这些成体干细胞存在于我们的许多器官中,它们在其中提供恒定的细胞供应,以替代衰老和死亡的细胞。 |

在科学界,确定这些发育严格调控的干细胞如何摆脱其调控机制是一个重要的课题。先前科学家认为,肿瘤细胞主要进行糖酵解反应,无需氧化代谢,近日有一项新的研究发现,果蝇神经干细胞肿瘤居然具有高度的氧化性,与正常细胞相比耗氧率更高。
该研究于9月10日发表在国际顶级学术期刊《细胞》(Cell),题为“Oxidative Metabolism Drives Immortalization of Neural Stem Cells during Tumorigenesis”。该研究发现,由线粒体膜融合介导的氧化磷酸化和NADH / NAD +代谢增加,会促使肿瘤永生。

图 文章发表 来源:《Cell》
肿瘤发生过程中的一个关键步骤是驱动肿瘤细胞发生的机制,它触发了它们成为肿瘤细胞的命运。迄今为止,科学家主要是通过研究肿瘤抑制基因MYC、p53或KRAS,在基因调控水平上进行癌症相关研究。其中,与正常细胞相比,肿瘤细胞会发生代谢变化是众所周知的,但是人们尚不清楚这些变化是肿瘤细胞永生化的结果还是其原因,因此,这是Knoblich团队最新研究的重点。
研究人员选择了黑腹果蝇(Drosophila melanogaster)作为肿瘤模型,这是被人类研究得最彻底的生物之一,上世纪70年代人们就发现了其体内存在抑癌基因突变。因此这一简单的模式生物可以作为强有力的工具,来促进人类基因的进一步研究。在该研究中,科学家们利用果蝇观察到肿瘤起始细胞成为永生细胞,并通过遗传方式操纵这一过程的确切时间点。由于哺乳动物肿瘤的复杂性,这并不易实现。
IMBA小组组长兼科学总监Jürgen Knoblich解释说:“我们使用了果蝇神经干细胞(NSCs)肿瘤模型,该模型是由耗竭性Brat肿瘤抑制因子诱导的。通过使用该模型,我们研究了新陈代谢在Brat肿瘤细胞永生化中是否发挥积极作用。我们在果蝇中的发现将用作人类细胞后续研究的基础,并为人类癌症的机理研究奠定基础。”
事实上,研究人员发现Brat肿瘤具有高度氧化性,与正常大脑相比,其耗氧率更高。由于科学界广泛认为,肿瘤细胞主要进行不耗氧的糖酵解反应,因此这一发现十分令人惊讶。
该研究另一个令人振奋的发现是,Knoblich团队的研究显示,氧化代谢是一种线粒体氧依赖性生物能途径,在肿瘤细胞永生化过程中起关键作用。该研究的第一作者,Knoblich实验室的博士后Fran?ois Bonnay解释道:“我们注意到,在肿瘤发生过程中,线粒体膜被融合了,线粒体形态的这种急剧变化导致氧化磷酸化效率的提高,这解释了为什么我们发现NAD +和NADH的含量增加,这是生物能量学中的两个关键分子。”
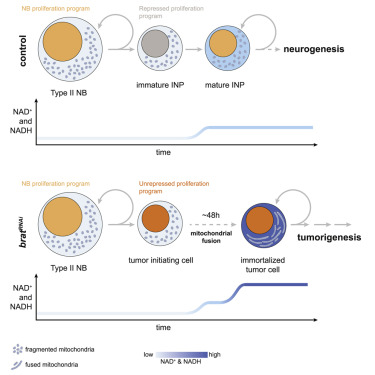
图解摘要
通过进一步的实验,科学家发现,在果蝇大脑中,确实发生了由线粒体融合介导的氧化磷酸化和NADH / NAD +代谢增加,这对于肿瘤细胞永生是绝对必要的。
“我们的发现推翻了先前关于这些肿瘤生物学的概念,并提出了一系列令人兴奋的后续问题,包括我们刚刚在果蝇中发现的机制是否也适用于哺乳动物肿瘤。我们还将努力解决的问题是, NADH / NAD +代谢如何精确地促进肿瘤细胞永生化,它是通过信号传递还是通过表观遗传改变来实现的?我们很高兴能够在这一领域开展工作。”(转化医学网360zhyx.com)
参考资料:
【1】https://medicalxpress.com/news/2020-09-fusion-immortalization-tumor-cells.html
【2】https://www.cell.com/cell/fulltext/S0092-8674(20)30947-8?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867420309478%3Fshowall%3Dtrue <https://www.cell.com/cell/fulltext/S0092-8674(20)30947-8?_returnURL=https://linkinghub.elsevier.com/retrieve/pii/S0092867420309478?showall=true
 腾讯登录
腾讯登录


还没有人评论,赶快抢个沙发