最新!香港大学研究发现胃癌治疗新机制
| 导读 | 由于缺乏生理和治疗相关模型,控制5-氟尿嘧啶和顺铂(5FU + CDDP)耐药性的可靶向驱动因素仍然难以捉摸。 |
近日,香港大学研究人员在《Nature Communications》发表论文“ADAR1-mediated RNA editing of SCD1 drives drug resistance and self-renewal in gastric cancer”,研究发现 ADAR1/SCD1 轴通过增强脂滴形成来中和化疗诱导的 ER 应激来控制化疗耐药性。

https://www.nature.com/articles/s41467-023-38581-8
研究背景
胃癌(GC)是一种治疗顽固性疾病,2020 年死亡人数超过 750,000 人。为了对抗气相色谱,除手术切除外,还经常进行5-氟尿嘧啶(5FU)和铂类联合化疗。事实上,与单独手术相比,5FU和顺铂(CDDP)联合使用围手术期的其他化疗可以提高生存率。然而,获得性化疗耐药性的出现最终会削弱长期临床益处。驱动化学耐药性的无数机制,加上构成各种亚型的GC,掩盖了靶标的识别以克服化学耐药性。此外,大多数研究化学耐药性的实验都是用单一化疗进行的,这与临床环境中通常应用的联合化疗相矛盾。目前,已经建立了各种组织学和分子分类;然而,亚型特异性脆弱性在临床进展方面相对未得到利用。因此,识别亚型特异性新靶点以规避联合化疗耐药性的需求尚未得到满足。
癌细胞系一直是了解化学耐药性的机制研究的核心。然而,体外培养时间的延长加上关于它们来源的肿瘤信息不足,挑战了这些细胞系与肿瘤生理状况的相似程度。因此,使用忠实地反映组织学和分子特征的GC患者来源的类器官培养物,以及它们来源的患者的药物反应,可能会阐明未报告的调节化疗耐药性的机制见解。
研究进展
在本研究中,研究人员建立了5FU + CDDP耐药肠道亚型GC患者来源的类器官系。JAK/STAT信号及其下游腺苷脱氨酶作用于RNA 1(ADAR1)被证明在耐药系中同时上调。ADAR1以RNA编辑依赖的方式赋予化学抗性和自我更新。WES 与 RNA-seq 偶联可鉴定抗性系中超编辑脂质代谢基因的富集。在机制上,ADAR1介导的硬脂酰辅酶A去饱和酶(SCD1)的3'UTR上的A-to-I编辑增加了含KH结构域,RNA结合,信号转导相关1(KHDRBS1)的结合,从而增强了SCD1 mRNA的稳定性。
因此,SCD1促进脂滴形成,以减轻化疗诱导的ER应激,并通过增加β连环蛋白表达来增强自我更新。SCD1的药理学抑制消除了化学耐药性和肿瘤起始细胞频率。临床上,ADAR1 和 SCD1 的高蛋白质组学水平或高 SCD1 编辑/ADAR1 mRNA 特征评分预示着预后较差。我们一起揭示了一个规避化学耐药性的潜在目标。
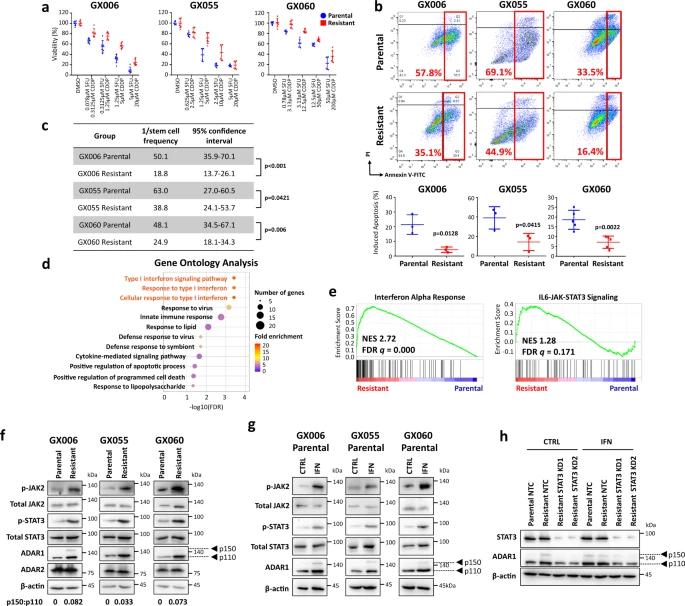
5FU + CDDP耐药胃类器官表现出干扰素/ JAK / STAT信号激活,导致诱导ADAR1表达。
研究意义
总的来说,研究发现 ADAR1/SCD1 轴通过增强脂滴形成来中和化疗诱导的 ER 应激来控制化疗耐药性。此外,我们的研究阐明了SCD1抑制的潜在临床意义。鉴于我们的工作重点是描述肠道亚型的化学耐药性,ADAR1 / SCD1轴是否有助于其他亚型的化学耐药性值得进一步研究(转化医学网360zhyx.com)。
参考资料:
https://www.nature.com/articles/s41467-023-38581-8
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发