CRISPR-Ca9全基因组脱靶效应检测系统在小鼠身上完成测试
| 导读 | 《自然》本周在线发表的一项研究,针对CRISPR–Cas9基因组编辑的全基因组脱靶效应的高效检测系统在小鼠身上完成了测试。研究成果有望促进基因组编辑从研究到临床的转化。 |

《自然》本周在线发表的一项研究In vivo CRISPR editing with no detectable genome-wide off-target mutations中,针对CRISPR–Cas9基因组编辑的全基因组脱靶效应的高效检测系统在小鼠身上完成了测试。研究成果有望促进基因组编辑从研究到临床的转化。
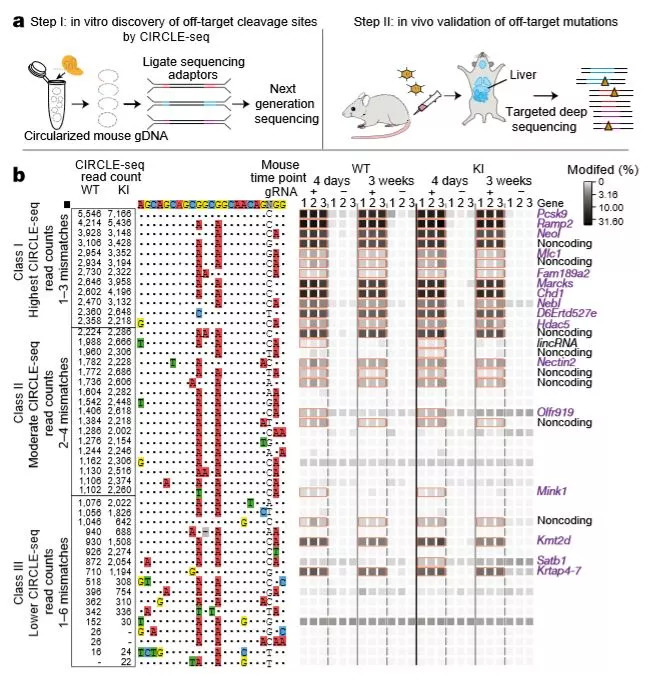
VIVO的概述和验证
Akcakaya et al.
CRISPR–Cas9基因组编辑被认为是人类医学史上具有巨大潜力的创新技术,但只有完全识别并消除额外的非目标(脱靶)突变,这项技术才能实现临床应用。脱靶突变是指CRISPR–Cas9复合物附着在基因组的多位点上,并切割了错误的DNA片段。检测这种突变的系统必须在体外以及整个生物体内都进行测试。
美国麻省总医院的J. Keith Joung,瑞典阿斯利康的Marcello Maresca及同事描述了一种灵敏度较高的“体内脱靶验证”(verification of in vivo off-targets,VIVO)系统,可以检测CRISPR–Cas9在生物体中的脱靶突变。VIVO会事先识别出潜在的脱靶位点,在基因组编辑后再确认这些位点中是否有位点发生了改变。
作者在小鼠肝脏中检测了该系统的准确度,方法是设计出靶向小鼠体内Pcsk9基因的不同的向导RNA(gRNA),包括混杂性(可以靶向多位点)的gRNA和特异性更高的gRNA。作者证实VIVO不仅能检测到混杂性gRNA诱导的数十种脱靶突变(包括发生率仅为0.13%的突变),而且正确设计的gRNA并不会带来任何可检测到的脱靶突变。
作者认为,VIVO 为定义基因组编辑在实际应用中的脱靶效应设立了重要标准,并证实了设计出特异性极高的gRNA的重要性。ⓝ
Nature|doi:10.1038/s41586-018-0500-9
原论文
In vivo CRISPR editing with no detectable genome-wide off-target mutations
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发