Cas9和AAV一相逢,便创造出许多奇迹,华人科学家高光坪在基因治疗领域取得重大突破
| 导读 | CRISPR/Cas9基因编辑在治疗遗传病上有着巨大的应用前景,腺相关病毒(AAV)由于其高安全性以及稳定长效表达,被视为最有前景的基因治疗载体。基于CRISPR/Cas9的AAV载体无疑是体内基因治疗最理想、最具前景的方式。 |
BioWorld: CRISPR/Cas9基因编辑在治疗遗传病上有着巨大的应用前景,腺相关病毒(AAV)由于其高安全性以及稳定长效表达,被视为最有前景的基因治疗载体。基于CRISPR/Cas9的AAV载体无疑是体内基因治疗最理想、最具前景的方式。
金风玉露一相逢,便胜却人间无数。
8月14日,麻省大学医学院高光坪教授团队在Nature Biotechnology杂志发表题为:Cas9-mediated allelic exchange repairs compound heterozygous recessive mutations in mice的研究论文(图1),该研究首次通过AAV介导的CRISPR/Cas9,无需外源基因模板,修复多突变的杂合型小鼠隐性遗传病模型,为进一步临床应用提供了新的策略。
 图1(图片来源:本论文)
图1(图片来源:本论文)
介绍该论文前,我们先介绍一个概念:复合杂合突变(compound heterozygous mutations)。
复合杂合突变,也就是双等位突变,一对同源染色体上的等位基因都发生了突变,且突变位点又不一样(图2)。
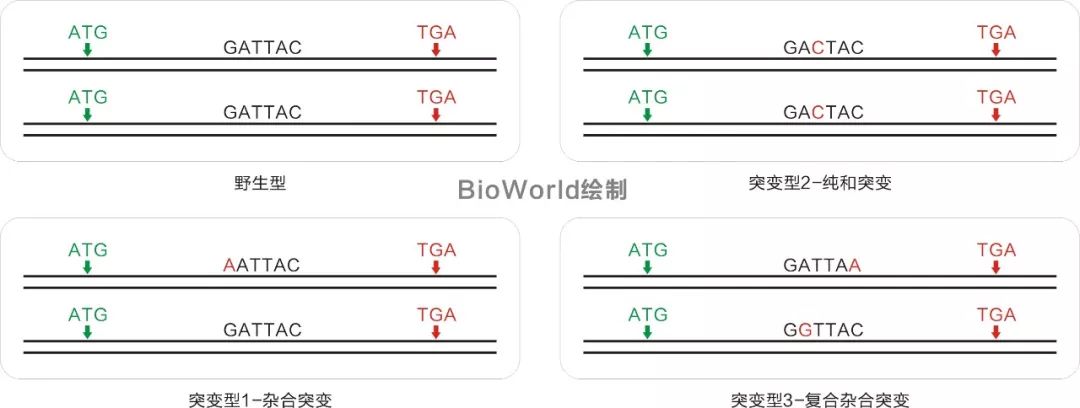
图2(图片来源:BioWorld绘制)
CRISPR/Cas9基因编辑在治疗遗传病上有着巨大的应用前景,通过外源DNA模板进行同源重组修复(HDR)可以单独校正突变基因。但是许多隐性遗传病涉及复合杂合突变,例如FAH基因中有超过95种已知突变可引起I型遗传性酪胺酸血症(HT1)。不依赖于突变的基因修复策略可以避免递送外源DNA模板,从而大大简化了治疗方法的开发。
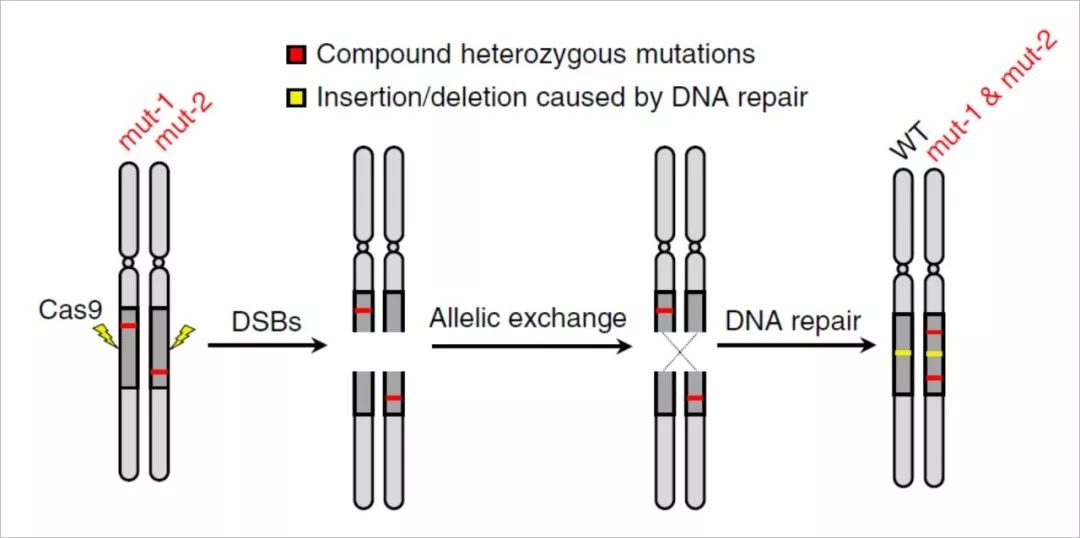
图3(图片来源:本论文)
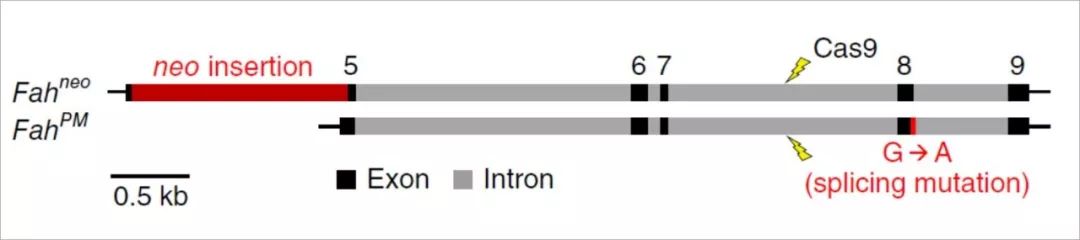 图4(图片来源:本论文)
图4(图片来源:本论文)
mut-1、mut-2是位于同源染色体上等位基因上不同突变位点,Cas9在sgRNA引导下,对这一对同源染色体均进行双链断裂(DSBs),DNA修复时进行了等位交换,从而形成了一条野生型染色体,一条同时有mut-1、mut-2的突变型染色体(图3)。由于该遗传病为隐性遗传病,拥有野生型染色体后不再表现出疾病表型。
设计sgRNA时,靶向两个突变位点间的内含子区域(图4),避免了Cas9切割后修复造成的编码蛋白序列的突变。
该方法的优势:单个验证的sgRNA足以修复多个不同突变;sgRNA可以靶向内含子区域,避免编码蛋白序列被破坏;无需外源DNA模板。
通讯作者简介
 高光坪教授
高光坪教授
高光坪:全球基因治疗领域领导者之一,美国基因与细胞治疗学会主席、麻省大学医学院教授、Horae基因治疗中心主任、Human Gene Therapy杂志主编、中国“千人计划”专家、生物制药企业Voyager Therapeutics的创始人之一,研发的治疗Canavan disease(海绵状脑白质营养不良病)的AAV基因治疗药物已被FDA批准并进行了首例"Expanded Excess" 临床应用。
论文链接:
https://www.nature.com/articles/nbt.4219(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发