突破性研究!清华大学李寅青/张学工/朱明团队揭示基因编辑副作用的分子机制,提出三种可最小化干扰、保全细胞功能的新型编辑策略
| 导读 | 研究所提供的“减震”策略为设计更安全、更精准的下一代基因编辑疗法提供了直接可行的路线图。 |
近日,清华大学李寅青/张学工/朱明团队一项发表于国际知名期刊《Cell Stem Cell》的研究揭示了CRISPR-Cas9基因编辑技术一个此前被忽视的重大副作用:即便在远离基因调控元件的非编码区进行编辑,也可能广泛扰动染色质三维结构,导致干细胞身份丢失。这项研究不仅阐明了其分子机制,更为重要的是提出了三种可最小化此类干扰、保全细胞功能的新型编辑策略,为基因编辑迈向更安全、更广泛的临床应用扫除了一大障碍。
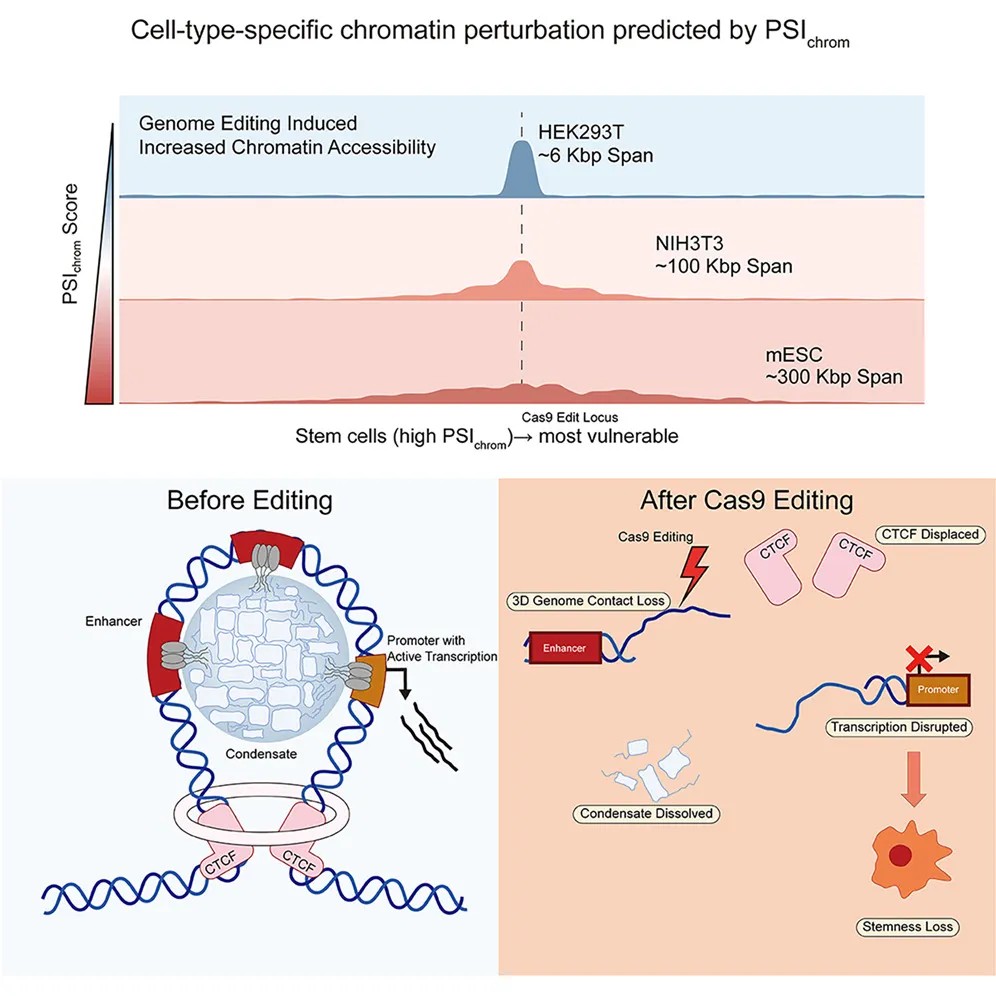
图形摘要
核心发现:远距离编辑的“蝴蝶效应”
基因编辑,尤其是CRISPR-Cas9技术,已被视为治疗遗传疾病的革命性工具。然而,超过97%的人类基因组是非编码区,其中密布着维持细胞身份的关键调控元件。传统安全评估主要关注编码区的脱靶突变,对非编码区编辑的长期影响知之甚少。
研究发现,在神经干细胞和小鼠胚胎干细胞中,即使CRISPR-Cas9的切割位点距离最近的调控元件有数万碱基之遥,仍会引发干细胞过早分化,丧失其“干性”。通过研究团队自主研发的AR-seq技术,研究人员首次在单次实验中同步检测了编辑后细胞的染色质可及性与基因表达变化。结果显示,编辑引发的染色质开放性改变具有细胞类型特异性,而以干细胞为代表的、具有高度“干性”的细胞所受影响最为剧烈,扰动范围可跨越数十万碱基。
机制揭秘:局部损伤,全局失调
研究进一步深入机制,发现局部DNA的切割损伤,会破坏依赖CTCF蛋白和相分离凝聚体的染色质高级结构。这种三维基因组架构的紊乱,导致了远距离的转录调控网络“重编程”,最终动摇了维持干细胞身份的核心基因表达程序,引发细胞身份丢失。
解决方案:三大策略精准“减震”
面对这一挑战,研究团队开创性地提出了三种可显著减少染色质扰动、保护细胞身份的优化方案:
-
距离感知的sgRNA设计:在设计引导RNA时,主动规避靠近关键调控元件(如CTCF结合位点)的区域。
-
药物抑制DNA末端切除:使用药物(如MRE11抑制剂)减弱DNA双链断裂后的末端切除过程,从源头上限制染色质结构的破坏范围。
-
采用替代编辑系统:使用不产生DNA双链断裂的碱基编辑系统,可几乎完全避免由切割引发的广泛染色质扰动。
从研究意义与未来展望
这项研究填补了基因编辑技术安全性评估的关键空白,首次系统揭示了编辑行为对基因组三维调控网络的深远影响。它警示,在干细胞治疗、器官再生等对细胞身份完整性要求极高的领域,进行非编码区编辑时必须慎之又慎。同时,研究所提供的“减震”策略为设计更安全、更精准的下一代基因编辑疗法提供了直接可行的路线图。(转化医学网360zhyx.com)
原文链接:
https://www.cell.com/cell-stem-cell/abstract/S1934-5909(26)00038-X
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发