2021年CTC临床应用进展 | 国内指南及共识
| 导读 | 在刚刚过去的2021年CTC在肿瘤诊疗的临床应用得到了进一步的挖掘和验证,业界对CTC在肿瘤精准诊疗的价值也有了更深的认可,今天就和大家一起回顾2021年我国CTC临床指南和共识有哪些更新。 |

CTC能够一定程度反映实体肿瘤的情况,可以作为补充手段进行病理诊断、疾病监测、分子测序等。不仅可以动态监测,还可以用于判断预后,其应用已经从数目走向了分子分型和细胞测序时代。

CTC检测有助于正确判断疾病临床分期,选择合适的治疗方案,可指导个体化治疗、监测肿瘤复发与转移、判定治疗疗效及预测预后生存,同时也是分析耐药分子机制及解决肿瘤异质性的一种手段。
国内专家共识

为规范CTC检测的合理应用,中华医学会检验医学分会分子诊断学组发布了《循环肿瘤细胞临床应用与验室检测专家共识》,该共识刊登于2021年11月的《中华检验医学杂志》。共识系统规范了CTC在临床实践中的关键问题,标志着CTC检测逐步进入临床普及阶段。
关于CTC的分析技术,该共识提到采用适配体技术和靶向PCR检测肿瘤细胞表面叶酸受体的表达可间接反应CTC的水平,具有高回收率和高敏感性的优势,是国家药品监督管理局批准的首个肺癌CTC检测方法。
该共识共计10条,涵盖了CTC临床应用、检测技术及质量管理,具体内容如下:
CTC计数的临床应用
共识1:CTC计数可用于乳腺癌、前列腺癌、结直肠癌、肝癌等实体肿瘤的疗效评价和预后评估,应结合具体肿瘤类型和CTC检测方法选择合适的判断阈值;追踪手术前后或综合治疗过程中CTC的动态变化可为肿瘤疗效评价和预后评估提供实时监测信息。
共识2:CTC计数可提示肿瘤转移风险和辅助肿瘤分期,联合CTC计数和影像学、病理学、血清学特征参数有助于更准确地评估肿瘤状态和疾病进展;不建议单独以CTC计数作为肿瘤早期筛查和诊断的工具。
CTC分子分型的临床应用
共识3:CTC分子分型可为全面评估肿瘤状态和肿瘤精准诊疗提供重要的实时信息;基于治疗靶标的CTC分型分析有助于提示药物疗效从而指导治疗决策,如ARV7(前列腺癌内分泌治疗)、HER‑2/EGFR/KRAS(靶向用药)、PD‑L1(免疫治疗)等。
共识4:CTC‑EMT分型的临床应用价值在多种肿瘤类型研究中得到证实,结合CTC计数和EMT分型及其动态变化可辅助肿瘤分期、复发风险评估及预后预测;针对肿瘤细胞干性和代谢特征的CTC功能分型有助于反映CTC的生物学转归和疾病的发展,是未来泛癌种CTC分子分型发展的前沿方向。
共识5:CTC有多种存在形式,包括单个细胞、CTC簇或CTC与其他血液成分(白细胞、血小板、巨噬细胞等)聚集成团,CTC细胞团检出率的提高有赖于检测方法的进一步优化;分析CTC的存在形式有助于揭示CTC与循环中血细胞、免疫细胞的相互作用,阐明CTC免疫逃逸和转移播散的机制,是CTC检测领域重要的探索方向。
CTC下游分析的临床应用
共识6:CTC体外培养、单细胞测序等下游分析是CTC检测领域的前沿方向,也是精准医学时代CTC临床应用的重要趋势;未来CTC检测技术的进步应着重突破CTC单细胞测序的瓶颈问题,探索单细胞CTC高保真核酸扩增及文库构建等创新技术,以促进CTC单细胞分析的发展和应用。
CTC检测技术
共识7:不同CTC分离与富集技术各有优缺点,实验室应结合应用目的和后续鉴定与分析的要求选择合适的方法;实验室应在充分评估所选方法的检测效能的基础上开展CTC分离与富集。
共识8:CTC鉴定与分析技术的选择应综合考虑上游分离富集技术的特点和下游应用的目的,根据肿瘤类型选择合适的标志物可提高CTC检测的准确性,结合细胞功能特征分析可丰富CTC检测的层次以适应临床诊疗的多种需求;实验室应在充分评估所选方法分析性能的基础上进行CTC鉴定与分析。
CTC实验室检测的质量管理
共识9:实验室开展CTC检测前应对所选分析系统进行性能验证,属于实验室自建方法的分析系统还应根据相关要求进行其他参数的性能确认;应注意所选CTC分析系统的适用范围,跨癌种应用时应考虑到不同起源、不同病理类型肿瘤细胞的理化性质不尽相同,须进行充分的性能验证和临床观察研究。
共识10:严格的质量管理是保证CTC检测结果准确、可靠的关键。实验室应针对CTC检测的各个关键环节,建立完善的质量管理体系以规范分析前、分析中及分析后的操作流程,并做好检测结果解读与临床沟通工作,以保障CTC临床应用的有效性及实用性。

2021年CTC临床应用进展 | FR+CTC 研究及数据
FR+CTC作为目前国内获得NMPA 第三类注册证的CTC检测相关产品中唯一涵盖了CTC富集、分析及所需校准品、质控品的CTC一体化检测试剂盒,积累了大量临床研究数据和真实世界数据,下面就来回顾2021年FR+CTC发表在SCI期刊的研究成果和数据。
肺癌 - 淋巴结转移(N分期)预测
同济大学附属上海市肺科医院一项纳入2821例肺腺癌患者的回顾性分析发现(Small Methods 2021, 2100152),术前FR+CTC水平可有效区分N1亚组(N1a和N1b)和N2亚组(N2a1、N2a2和N2b),同样可清晰区分各亚组中不同淋巴结受侵数量的患者群体。此外,单个淋巴结转移和多个淋巴结转移与FR+CTC之间的同样密切相关(N1a Vs. N1b,N2a Vs. N2b)。同时在N分期预测模型中纳入FR+CTC后可提高预测准确度,该模型的AUC均值为0.786。该研究证实术前FR+CTC检测可有效预测肺腺癌患者的淋巴结转移,从而可为制定个性化的治疗方案提供依据。
FR+CTC可区分N2亚组中不同淋巴结受侵数量
肺癌 – 预后预测
复旦大学附属肿瘤医院长达7年的前瞻性研究发现(Front. Oncol. 2021; 10: 621435),非小细胞肺癌(NSCLC)患者术前FR+CTC水平,可在传统病理分型的基础上,对患者术后复发风险进一步细分,其中病理低风险/FR+CTC高水平的患者5年无复发率(RFS)明显低于病理低风险/FR+CTC低水平的患者(58.5% Vs. 87.5%),提示可根据NSCLC患者术前FR+CTC水平进行复发风险细分,为临床决策提供多维度的风险预测因子。
不同术前FR+CTC水平/病理分组的RFS
另一项同济大学附属上海市肺科医院的回顾性分析(Transl. Lung Cancer R. 2021; 10(2): 995-1006)则聚焦于FR+CTC与早期NSCLC患者预后的相关性,研究中84.1%(292/347)为0-I期NSCLC患者。数据证实,术前FR+CTC水平与术后复发和转移部位密切相关(p<0.05), 在各类RFS的独立影响因子(术前FR+CTC水平、T分期、淋巴结转移、性别)中,术前FR+CTC水平对NSCLC患者的RFS有最佳的预测价值(HR:5.489),提示FR+CTC可用于辅助发现早期NSCLC患者中复发和转移高风险人群。
术前FR+CTC是早期NSCLC预后预测因子
前列腺癌 - 早期发现
北京大学肿瘤医院关于FR+CTC在前列腺癌的检测准确度以及不同tPSA和f/tPSA分组中FR+CTC水平差异的研究(Front.Oncol. 2021; 11: 708214)发现,在tPSA<10ng/mL、f/tPSA<0.16的前列腺癌患者中,FR+CTC相比tPSA具有更优的检测性能(AUROC 0.912 Vs.0.857),FR+CTC在前列腺癌检测中具有较高的准确度,尤其对于灰区的可疑前列腺癌患者,FR+CTC具有更优的表现。
FR+CTC和tPSA在tPSA<10 ng/mL、f/tPSA<0.16患者的检测性能
乳腺癌 - 早期发现及疗效监测
武汉大学人民医院探讨FR+CTC在乳腺癌诊断和疗效监测的临床价值的研究中(J Clin Lab Anal. 2021 Dec; 17: e24180),FR+CTC检测乳腺癌的灵敏度为63.33%,特异性为93.75%,AUC为0.778,优于乳腺癌常规肿瘤标志物,同时FR+CTC联合乳腺癌常规肿标可显著提高乳腺癌的诊断效率(联合AUC为0.887)。同时发现术后FR+CTC水平下降明显:术前中位值 13.20 FU Vs. 术后中位值 10.41 FU(p<0.05),提示FR+CTC水平可用于乳腺癌早期发现和疗效监测。
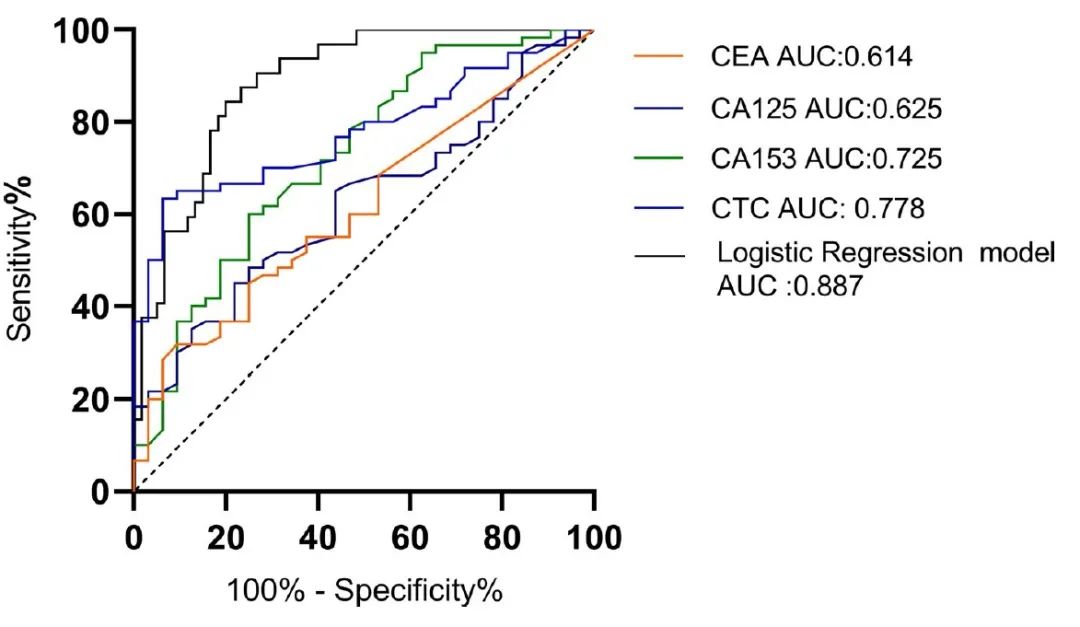
FR+CTC和常规肿瘤标志物在乳腺癌的检测性能
FR+CTC在各类肿瘤的检测性能
FR+CTC在各类肿瘤的检测累计近20万人次,在大部分肿瘤的检测灵敏度和特异性都在75%-90%之间,检测性能经临床大数据验证,是可靠的CTC检测技术。
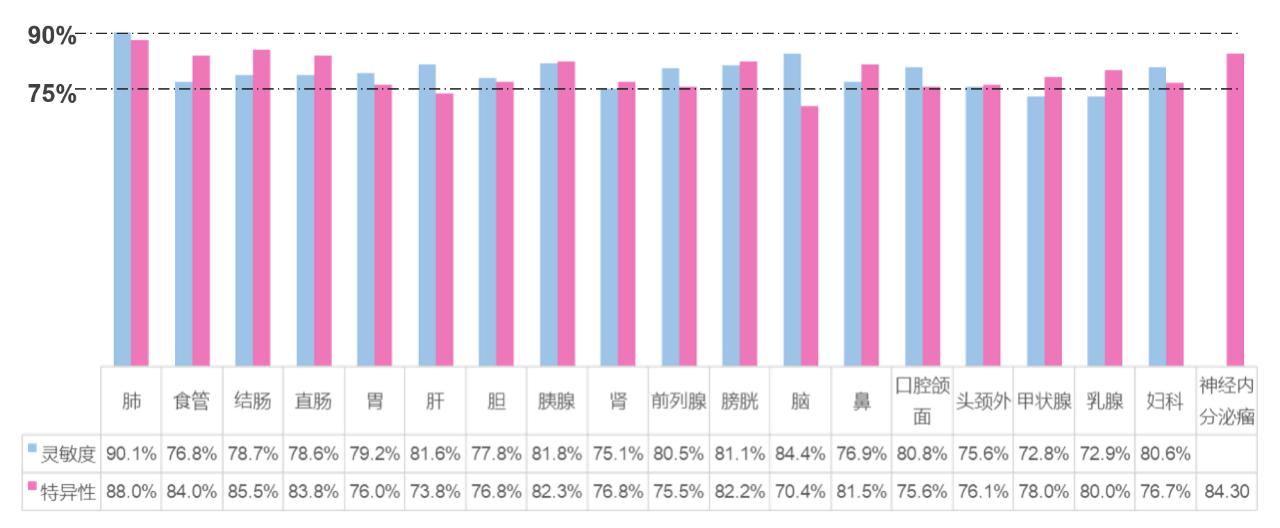
2021年FR+CTC在不同肿瘤的检测性能
2021年10月29日,国家药品监督管理局(NMPA)发布《体外诊断试剂分类规则》的公告(2021年第129号),提出用于肿瘤筛查、诊断、辅助诊断、分期等相关的试剂,包括配合使用的校准品、质控品都应按第三类体外诊断试剂管理。这也从法规层面对CTC检测技术和产品提出了新的要求。随着法规、指南和共识的逐步推进和落实,未来CTC检测在临床应用将日益规范。FR+CTC已积累了丰富的临床研究数据,证实对于肿瘤早发现、辅助诊断、复发监测、疗效监测以及预后预测都有独特的临床价值,可为肿瘤患者的精准管理提供准确可靠的依据。
关于格诺
格诺生物是“精准医疗”领域里致力于肿瘤诊断技术创新的先行者,专注于打造“液体活检”的完整解决方案,旗下产品包括一系列自主开发的基于CTC、ctDNA、外泌体等各类样本的全癌种诊断试剂。格诺叶酸受体细胞检测试剂盒是唯一获得NMPA批准的III类注册证的CTC富集与分析一体化产品。基于最大临床样本量的肺癌数据验证,其灵敏度为80.2%,特异性为88.0%,I期患者检出率为67.2%。格诺GenoploRare试剂盒基于ARMS-Plus技术定量检测血浆ctDNA的EGFR突变,灵敏度可达万分之一,远高于同类产品。格诺OncoploRare试剂盒为基于NGS技术的ctDNA多癌种检测产品,兼具高建库效率、高灵敏度、高性价比等多项优势。格诺“液体活检”产品还包括高效CTC富集试剂盒CytoPrep、高效cfDNA富集试剂盒GenoPrep、CTC富集芯片CytoTron、多基因联合肠癌甲基化检测试剂盒EpiploRare等等,以及基于CTC富集后的ICC、IHC、IF、FISH、RNASeq等一系列检测产品。

关注液体活检CN,了解更多

 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发