【重磅】朱焕章团队报告趋化因子受体修饰CART可提高其体内抗肿瘤活性
| 导读 | 复旦大学朱焕章教授团队首次将趋化因子受体联合CAR T细胞治疗应用于非小细胞肺癌(NSCLC)的研究,为推进实体瘤的临床治疗带来了新的希望。 |
近日,复旦大学朱焕章教授团队报道了在NSG小鼠肺癌CDX模型中,趋化因子受体CCR2b可以促进靶向间皮素的CAR T细胞向肿瘤组织的迁移,从而增强其抗肿瘤功能,这是首次将趋化因子受体联合CAR T细胞治疗应用于非小细胞肺癌(NSCLC)的研究,为推进实体瘤的临床治疗带来了新的希望。
该研究发表在国际著名杂志《Frontiers in Immunology》上,题为“Chemokine receptor CCR2b enhanced anti-tumor function of chimeric antigen receptor T cells targeting mesothelin in a non-small-cell lung carcinoma model”。

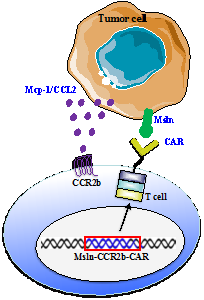
图1. 趋化因子受体CCR2b/CCR4增强Msln-CAR T细胞抗肿瘤模式图
通过transwell实验证明CCR2b及CCR4在体外可以促进CAR T细胞的迁移。将修饰后的肺癌细胞系与CAR T细胞共孵育,体外检测到高效的细胞杀伤及细胞因子分泌。
进一步构建了移植 A549-MLM 的 NSG 小鼠肺癌 CDX 模型,在肿瘤细胞移植 7 天后,小鼠随机分为 Msln-CCR2b-CAR、Msln-CAR 和PBS组,并进行 2 次效应细胞的移植治疗。在肿瘤细胞移植35天后,小鼠活体成像提示 Msln-CAR 组小鼠有 60%肿瘤细胞完全清除,而Msln-CCR2b-CAR 组达到 100%的清除率。与 PBS 组相比,CAR T 细胞治疗组肿瘤重量显著降低 (P<0.001)。肿瘤组织IHC分析表明CCR2b表达后使迁移浸润到肿瘤组织的CD3 T细胞数提高了2倍。

图2. NSG小鼠肺癌CDX模型中,CCR2b增强了Msln-CAR T细胞抗肿瘤作用
近几年来,朱焕章团队在基因编辑治疗的临床前研究方面取得一些进展。
2013年在国际上首次提出并证实基因编辑靶向切除HIV前病毒的“斩草除根”治疗策略的可行性 (Nucleic Acids Res., 2013, 41:7771-82),并获得基因编辑治疗疾病的首个中国发明专利;成功实现诱导型锌指核酸酶 (ZFN) 靶向切除近9.8 kb HIV前病毒 (Molecular Therapy-Nucleic Acids, 2018, 12, 67-74)。
2020年利用CRISPR-Cas9文库大规模基因敲除技术首次筛选到HIV-1潜伏相关的基因PEBP1 (EMBO Rep, 2020, e49305)。对于血液瘤及实体瘤的肿瘤免疫疗法也进行了研究,构建了靶向CD19、间皮素及EGFR的CAR T细胞,结合免疫检查点、趋化因子受体等从多个角度在人源化小鼠中增强了CAR T细胞的抗肿瘤功能。
论文链接:
https://www.frontiersin.org/articles/10.3389/fimmu.2021.628906/full?&utm_source=Email_to_authors_&utm_medium=Email&utm_content=T1_11.5e1_author&utm_campaign=Email_publication&field=&journalName=Frontiers_in_Immunology&id=628906
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发