【科普】铁死亡基础科普及谱领铁死亡研究专项服务方案
| 导读 | 铁死亡是一种铁依赖性的,区别于细胞凋亡、细胞坏死、细胞自噬的新型的细胞程序性死亡方式。 |

一、关于铁死亡,你可能首先需要知道这些:
1. 什么是铁死亡?
铁死亡(Ferroptosis)最早由哥伦比亚大学Brent R.Stockwell教授于2012年提出,是一种铁依赖性的,区别于细胞凋亡、细胞坏死、细胞自噬的新型的细胞程序性死亡方式。铁死亡是一种受调节的细胞死亡形式,其本质是谷胱甘肽的耗竭,谷胱甘肽过氧化物酶(GPX4)活性下降,细胞抗氧化能力降低,致使脂质过氧化反应增加,脂质活性氧(ROS)增多,最终引发铁死亡。
铁死亡的特征在于脂质过氧化的铁依赖性积累达到致死水平。当细胞胱氨酸运输蛋白受到抑制(如Erastin),胞内谷胱甘肽(GSH)会被耗尽,最终导致谷胱甘肽过氧化物酶(GPX4)失活和脂质过氧化积累,达到一定程度即可诱发细胞死亡,GPX4酶受到抑制(如RSL3)也可以直接导致这一作用。铁死亡的敏感性与许多生物过程紧密相关,包括氨基酸、铁和多不饱和脂肪酸代谢,以及谷胱甘肽、磷脂、NADPH和辅酶Q10的生物合成。
需要说明的是,目前很多抑制或缓解脂质过氧化的药物均可抑制铁死亡进程,包括亲脂性抗氧化剂和脂质过氧化抑制剂等等,但不能被凋亡或自噬抑制剂抑制。
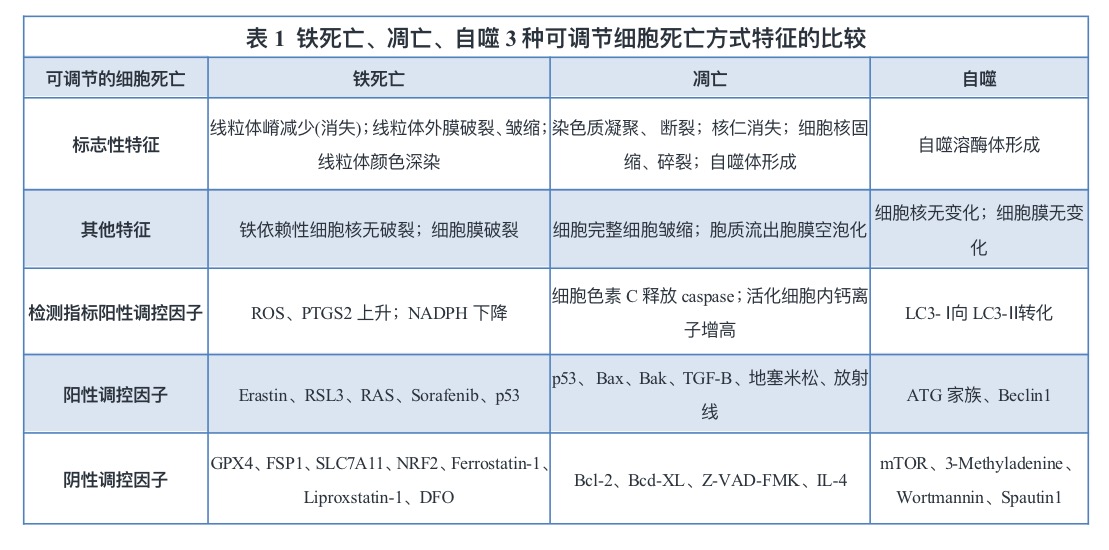
2. 铁死亡主要有以下几个特点:
(1) 细胞死亡过程中伴随着大量的铁离子的累积,同时还会出现脂质过氧化和ROS升高,也有一些调控铁稳态和脂质过氧化代谢等方面的基因发生变化。
(2) 在细胞的细微结构中,会出现比正常细胞小的线粒体,且线粒体膜皱缩,同时线粒体嵴减少或消失,外膜破碎,但细胞核中形态变化不明显。
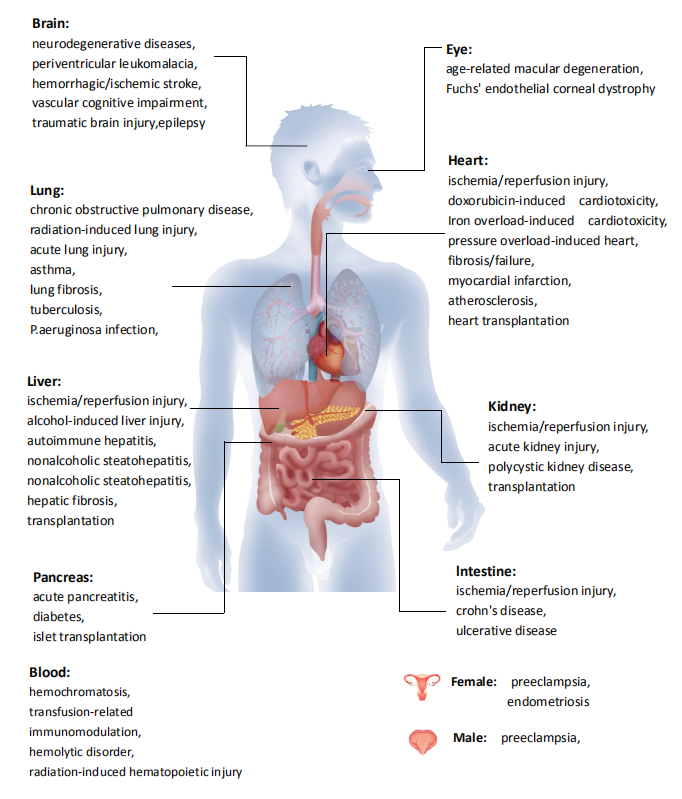
3. 铁死亡与疾病:
在疾病模型中验证铁死亡的干预手段将有助于我们更好地理解铁死亡参与到这些疾病中的作用。如研究显示,模拟 GPX4 活性降低(GPX4 单基因敲除)模型的小鼠可以健康长大,但在接受刺激时会出现更为严重的病理变化。另外也有研究报道,铁死亡诱导剂对抑制几种类型的癌症特别有效。笔者总结了铁死亡的研究对于以下疾病具有重要意义:
(1) 退行性疾病:阿尔茨海默病、帕金森病、亨廷顿病、佩梅病、肌萎缩侧索硬化症、多发性硬化症和弗里德赖希共济失调。
(2) 肿瘤和癌症抑制:如三阴性乳腺癌,弥漫性大 B 细胞淋巴瘤,肾脏和卵巢透明细胞癌,胰腺导管腺癌、肝细胞癌、神经母细胞瘤、肾上腺皮质癌、顺铂耐药头颈部癌和耐药急性髓系白血病等疾病。
(3) 心脑血管疾病:中风、脑出血、外伤性脑损伤等疾病。
(4) 局部缺血再灌注损伤和肾脏变性。
4. 如何调控铁死亡:
目前,对铁死亡的调控,主要集中在System Xc-、GSH代谢、谷胱甘肽过氧化物酶4(GPX4)活性调控和ROS生成等方面。
(1) System Xc-调控:
System Xc-由SLC3A2和SLC7A11二聚体组成,嵌于细胞膜表面。SLC7A11是发挥功能的主要亚基,可将胱氨酸转运入胞,用于合成GSH;因此,抑制SLC7A11表达可诱导铁死亡发生。p53作为一种抑癌基因,就是通过下调systemXC-组分SLC7A11的表达抑制细胞对胱氨酸的摄取,导致谷胱甘肽过氧化物酶活性降低,削减细胞抗氧化能力,增强细胞对铁死亡的敏感性。同时,研究发现,在人肿瘤细胞中SLC7A11过度表达,这种过表达能够抑制活性氧诱导的“铁死亡”,同时削弱p533KR介导的对肿瘤生长的抑制作用。
(2)GSH和GPX4调控:
研究认为GPX4是细胞生存的关键,也是铁死亡的核心调控蛋白,GPX4能降解小分子过氧化物和某些脂质过氧化物,抑制脂质过氧化。如果不能有效地被GPX4淬灭,磷脂氢过氧化物能够在过渡金属(如铁)存在的情况下引发催化反应,最终导致细胞死亡。研究发现,若细胞中GPX4表达下调则会对铁死亡更敏感;敲降GPX4即可诱导铁死亡发生;相反,若上调GPX4的表达,则会产生对铁死亡的耐受。丁硫氨酸亚砜胺(BSO)可抑制GSH合成、降低GPX4活性,导致铁死亡发生。RSL3可以直接与GPX4蛋白结合使其失活,诱导脂质ROS产生,导致细胞铁死亡发生。另外,过表达GPX4细胞表现出对RSL3的抵抗性,抑制其诱导的细胞铁死亡。
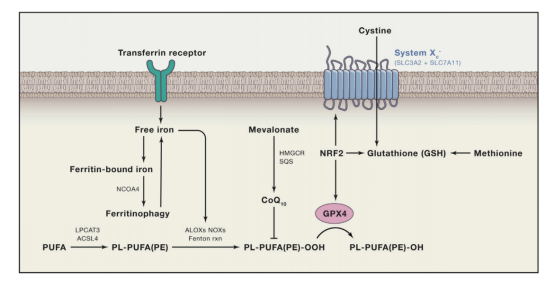
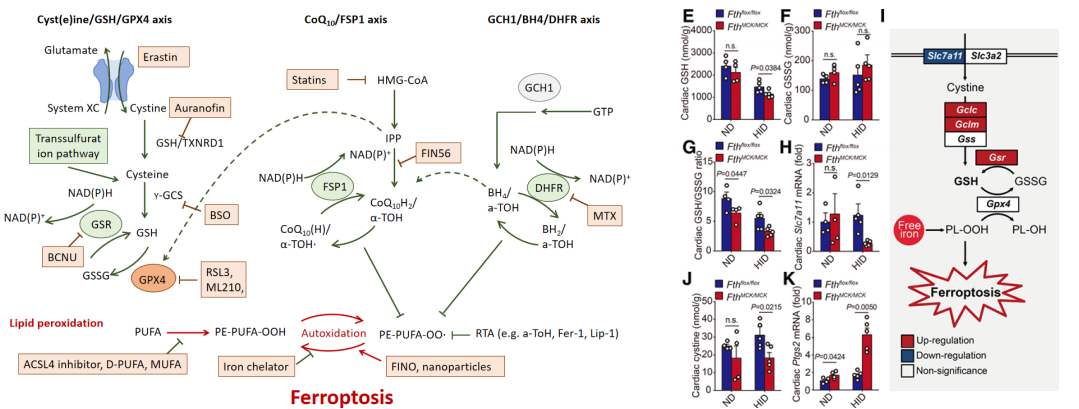
图2 铁死亡通路
(3)ROS调控:
诱导铁死亡发生均会导致细胞内脂质ROS升高,从而引起细胞死亡,这也是脂质抗氧化剂可抑制铁死亡的原因。线粒体作为含铁丰富(铁是线粒体氧化呼吸链必需离子)、产生ROS为主的细胞器,被认为是铁死亡发生的重要场所。它既是细胞内产生ROS的重要场所,其脂肪酸代谢又为细胞铁死亡提供特定的脂质前体。p53也能够通过ROS应答和“铁死亡”抑制肿瘤生长。
二、谱领生物的铁死亡相关代谢物检测分析专项服务方案:
精准的检测和分析铁死亡相关代谢物,对于生理、病理等多种生命科学研究具有重要意义。为了满足更多需求,并提供更优质、更快捷的服务,经过数月的努力,谱领生物将此前的服务方案进一步开发、改进和服务升级,并与铁死亡研究领域领军科学家浙江大学王福俤教授联合正式对外推出铁死亡相关代谢物检测分析服务。
1. 谱领生物服务优势:
(1) 采用谱领氧化脂肪酸和氧化还原代谢物钝化技术,使检测结果更加接近样本原生态,更加符合真实情况。
(2) 定量限低至 pg 级别,让更多成为可能。同时检测多种指标,更具性价比。
(3) 国际一流代谢组学服务团队,多年技术积累,上万例生物样本检测经验。
2. 服务内容:
(1) 氧化脂肪酸(Oxylipin)检测分析;
(2) 氧化还原代谢物(Redox metabolites)检测分析。
3. 各项服务简介:
(1) 氧化脂肪酸(Oxylipins)检测分析包含:
亚油酸(LA)、γ-亚麻酸(GLA)、dihomo-γ亚麻酸(DGLA)、花生四烯酸(AA),α-亚麻酸(ALA),二十碳五烯酸(EPA)和二十二碳六烯酸(DHA)及其相关的代谢途径的一百六十多种氧化脂肪酸代谢物。例:花生四烯酸(AA)代谢途径:
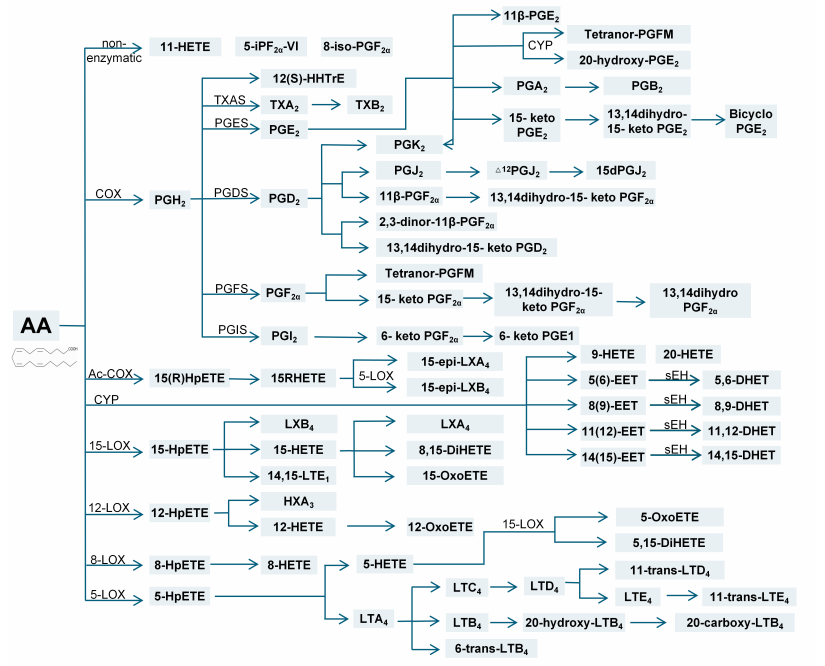
(2) 氧化还原代谢物(Redox metabolites)检测分析包含:
还原型谷胱甘肽(GSH)、氧化型谷胱甘肽(GSSG)、还原型烟酰胺腺嘌呤二核苷酸(NADH,还原型辅酶I)、氧化型烟酰胺腺嘌呤二核苷酸(NAD+,氧化型辅酶I)、还原型烟酰胺腺嘌呤二核苷酸磷酸(NADPH,还原型辅酶II)、氧化型烟酰胺腺嘌呤二核苷酸磷酸(NADP+,氧化型辅酶II)、半胱氨酸(Cysteine)、胱氨酸(Cystine)、谷氨酸(Glutamic acid)等。
4. 服务平台:

如您想进一步了解详情,也可添加下方谱领科研服务客服微信或拨打咨询热线:

参考文献:
[1] Brent R. Stockwell*, José Pedro Friedmann Angeli, Hülya Bayir, et al. Ferroptosis: A Regulated Cell Death Nexus Linking Metabolism, Redox Biology, and Disease[J]. Cell, 2017, 171(2):273-285.
[2] ZHENG Jiashuo, Conrad Marcus*. The Metabolic Underpinnings of Ferroptosis[J]. Cell Metabolism, 2020, 32(6):920-937.
[3] José Pedro Friedmann Angeli, Dmitri V. Krysko, Marcus Conrad. Ferroptosis at the crossroads of cancer-acquired drug resistance and immune evasion[J]. Nature Reviews Cancer, 2019, 19(7):405-414.
[4] Wan Seok Yang, Rohitha SriRamaratnam, Brent R. Stockwell*, et al. Regulation of Ferroptotic Cancer Cell Death by GPX4[J]. Cell, 2014, 156(1-2):317-331.
[5] GAO Minghui, Prashant Monian, PAN Qiuhui, et al. Ferroptosis is an autophagic cell death process.[J]. Cell research, 2016, 26(9):1021-1032.
[6] FANG Xuexian , CAI Zhaoxian , WANG Hao , et al. Loss of Cardiac Ferritin H Facilitates Cardiomyopathy via Slc7a11-Mediated Ferroptosis[J]. Circulation Research, 2020,127(4).
[7] Adedoyin. O, Boddu. R, Traylor. a, Agarwal. A, et al. Heme oxygenase-1 mitigates ferroptosis in renal proximal tubule cells. Am. J. Physiol. Ren, Physiol, 2018, 314: 702–714.
[8] Badgley, M.A., Kremer, D.M., Maurer, H.C., Olive,K.P., et al. Cysteine depletion induces pancreatic tumor ferroptosis in mice. Science, 2020,368: 85–89.

-
 游客2021-02-02 11:04:59铁爷
游客2021-02-02 11:04:59铁爷 -
 游客2021-02-02 11:03:43棒棒的
游客2021-02-02 11:03:43棒棒的 -
 游客2021-02-02 11:03:08太好了,我正打算学习,感谢感谢
游客2021-02-02 11:03:08太好了,我正打算学习,感谢感谢
 正在加载
正在加载 腾讯登录
腾讯登录