回顾MD Anderson在RPPA技术领域的开山之作‖中美联合在线研讨会
| 导读 | 中美联合在线研讨会邀请了美国贝勒医学院的Shixia Huang博士和中国非因生物的王楠博士一起来探讨RPPA技术的优势和面临的挑战,会议将于10月15日 上午09:30开始,期待您的参与! |

北京时间:2020年10月15日 上午09:30
RPPA(反相蛋白微阵列)技术是一种可靠的、成熟的、高灵敏和高通量的系统蛋白组学分析技术。这种分析方法的独特性,在于能够同时分析成百上千个样本(细胞或组织裂解物),并进行平行蛋白组学差异表达比对分析,包括其活化水平,例如磷酸化、甲基化、乙酰基化等,且具有其它高通量蛋白组学所不具备的定量优势。本次研讨会邀请了美国贝勒医学院的Shixia Huang博士和中国非因生物的王楠博士一起来探讨RPPA技术的优势和面临的挑战。

注册报名
扫描下方二维码进行注册报名,报名成功后从收到的邮件中点击链接登录

注册链接:https://quanterix.zoom.us/webinar/register/WN_QpRfaZilRuKd4AMGcIJ19A
如需更多信息请联系:fwmeng@nl17.com,18667018195
讲座开始之前带您一起回顾MD Anderson癌症中心在RPPA领域的开山之作
——Comprehensive molecular portraits of human breast tumours
(October 2012,Nature 490(7418):61;DOI: 10.1038/nature11412)
研究背景
乳腺癌是全世界范围内最常见的妇科肿瘤(如图1),每年有新增确诊超过130万例,每年死亡人数超过45万例。早期在临床分型上,这种高异质性的癌症根据雌激素受体表达水平(Estrogen Receptor, ER)、孕激素受体表达水平(Progesterone Receptor, PR)和 HER-2拷贝数增加来进行针对性的治疗方案及策略选择。对于荷尔蒙受体阳性的病人,主要采用内分泌疗法,对于HER-2过表达的病人,则采用以HER-2抑制剂(Herceptin)为主的靶向疗法,而对于荷尔蒙受体及HER2表达阴性的三阴性乳腺癌(Triple negative breast cancer TNBC)一线仍然采用以化疗为主的治疗方案。

大多乳腺癌的分子学研究都集中在数据量比较丰富的1个或2个技术平台,由于大规模平行测序技术的发展,越来越多的组学数据开始在乳腺癌中产出,包括了mRNA表达谱、DNA拷贝数分析、甲基化数据,microRNA表达。基因组学层面的分析与检测已经从实验室走向了临床应用,为乳腺癌的诊断与治疗提供了丰富的资源。而这仅仅是癌症精准医学的开始。“Comprehensive molecular portraits of human breast tumours”(图2)则是2012年TCGA项目利用多组学技术,对乳腺癌分子水平进行系统性、大规模研究的一个里程碑,这篇文章描述的内容被誉为医学界第一次运用高通量多组学技术、全面剖析乳腺癌分子分型的开元性工作,不计其数的科研和临床工作者都对其进行了深入的解读,以至于在发表后的两年内成为了除综述外引用次数最多的临床医学研究类论文之一。

TCGA的蛋白组学分支,在MD安德森系统生物学系Gordon Mills教授团队的带领下,运用RPPA技术,通过对403例乳腺癌样本中171个与癌症相关的蛋白及其磷酸化水平进行了相对丰度测定。这项分析在当时是纳入样本数最多、最大的一项乳腺癌分型蛋白组学分析,也因RPPA技术的加持,开创性的发现了一系列癌症系统蛋白组层面的新现象,并找到了多种潜在与药物治疗靶点、分子分型相关的蛋白组学信息,并关联到其它驱动基因,关键位点和高频突变。
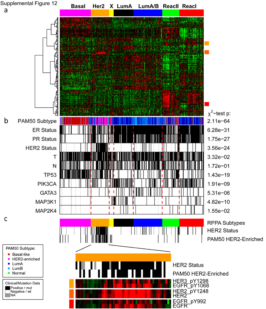
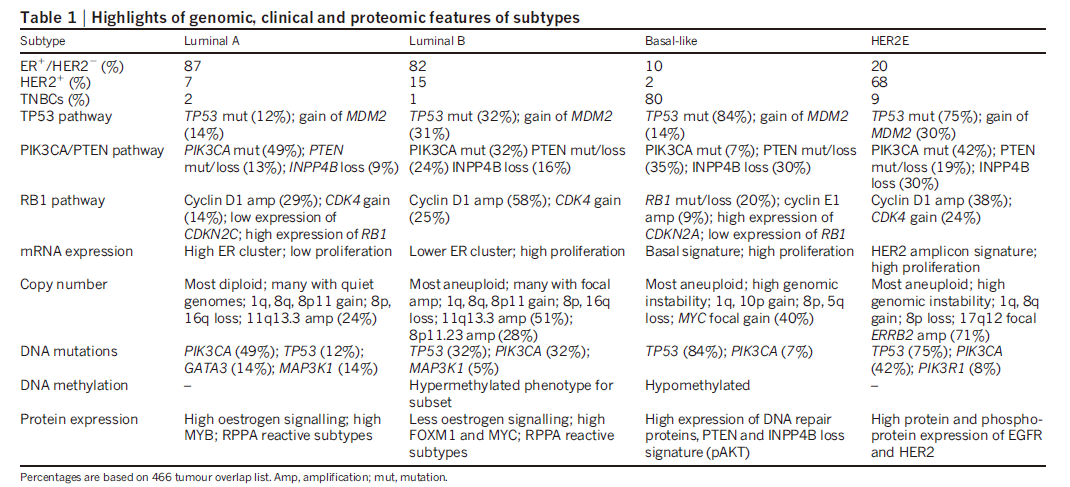
研究团队通过RPPA靶向蛋白组学分析,发现7个由蛋白组学定义的亚型。这些蛋白组定义的亚群与转录组分型高度一致,也验证了转录组层面的信息可以很好地体现在蛋白组尤其是功能蛋白组层面。深入分析表明,尤其是在HER2过表达亚型中,蛋白组学的信息高度一致,同时也反映在HER2以及EGFR的丰度和磷酸化水平上。在管腔型乳腺癌中,RPPA蛋白组学发现了高表达的ER,PR,AR,BCL2,GATA3以及INPP4B,这些蛋白与管腔A型具有高度关联。而在另一个由RPPA蛋白组学定义的组内,发现了高度异质性,这里面包括了A/B两种表型的样本。这个组含有高表达的与肿瘤微环境相关的蛋白以及肿瘤相关成纤维细胞蛋白( fibronectin, caveolin 1 and collagen VI.)。其中Reactive I型包含了大部分管腔A型,而Reactive II型包含了由RNA定义的各个亚型的混杂样本。通过前期病理学验证,这两个组别间并没有肿瘤细胞含量的显著差异,也说明该分型的可靠性。通过两个分子亚型的监督聚类分析,发现了在miRNA,DNA甲基化,突变,以及拷贝数变异层面无法将这两个组别区分开,而在mRNA转录组层面有着一定的关联。也证明了蛋白组层面信息,无论是在临床分型,治疗靶点探索中无可替代的重要性。(如图3)。
通过对同一样本的多组学分析,研究者还发现了一些亚型相关的突变在蛋白组层面即存在一定的关联性,也存在一定的差异性。如管腔A型中的高频PIK3CA突变并没有造成下游通路蛋白的高度磷酸化(pAKT,pS6,p4EBP1),而这个高频突变在三阴性和HER2阳性乳癌中呈现出高度过表达。TP53通路 在luminal A亚型中很大程度上是完整的,在侵袭性更强的luminal B亚型中通常是失活的;RB作为抑癌因子,在lunimal亚型的mRNA和蛋白层面都有表达,尤其是luminal A亚型,因此该亚型的预后通常也是最好的。(图4,图5)
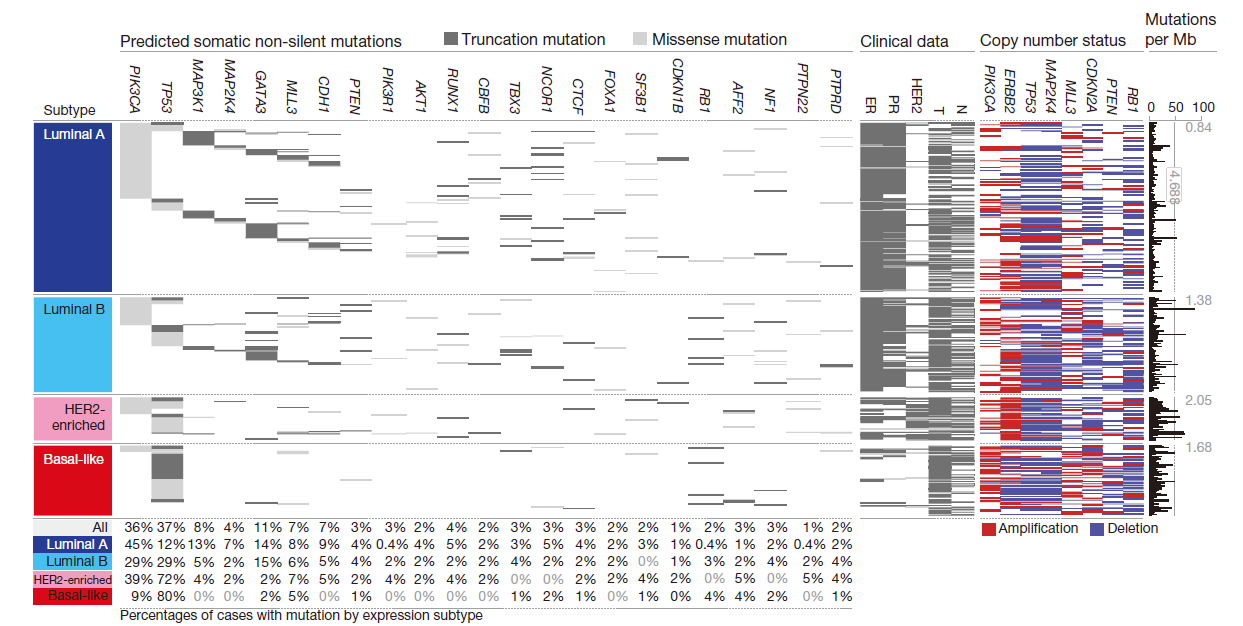
图4
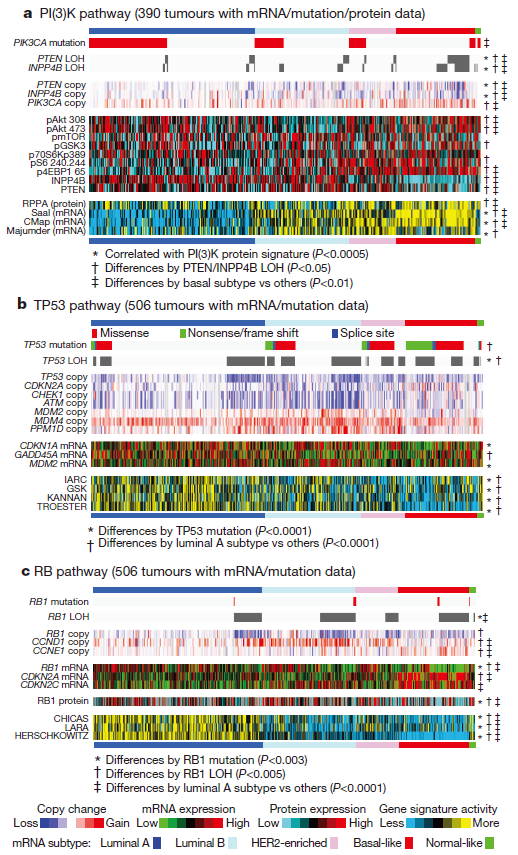
图5
在临床上,虽然已经验证了HER2阳性与DNA拷贝数变异相关,但HER2阳性病人也不完全由HER2分子分型决定。通过RPPA及mRNA表达谱,研究者确认了分子型与临床表型重合病人中的高度HER2/EGFR表达及磷酸化;利用蛋白表达分型,发现有50%的临床HER2阳性类型属于管腔型乳腺癌,也验证了至少存在2中临床亚型表征,为治疗提供了依据;而通过RPPA也发现了至少36种显著差异蛋白表达,这为两个临床HER2表型的亚型的生物标志物探索提供了新的思路。
这项开创性的多组学整合性分析,包括患者在基因与表观层面的改变都能归类到4种主要的乳腺癌分型中,不仅与基因组层面的趋同进化一致,就像在多种其他生物体中观察到的一样,而且也与乳腺癌克隆扩增和体内细胞选择的模式相一致,该模式能够用来解释在特定乳腺癌亚型中观察到的表型异质性(图6)。而RPPA蛋白组学信息不仅提升了多组学整合性分析的潜力,也发现了全新的与分子分型,治疗靶点相关的信息,为临床转化提供了更加强有力的证据(图7)。
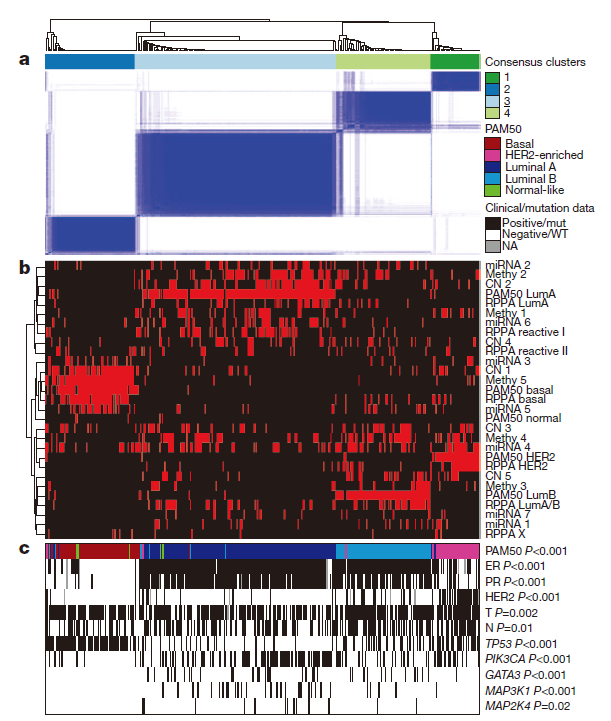
对6种技术平台数据进行整合分析发现,mRNA、RPPA与共分析分型有很强的相关性,说明其他几种信息量,包括像DNA拷贝数异常、DNA甲基化等都能够从基因表达层面与蛋白功能层面获取。
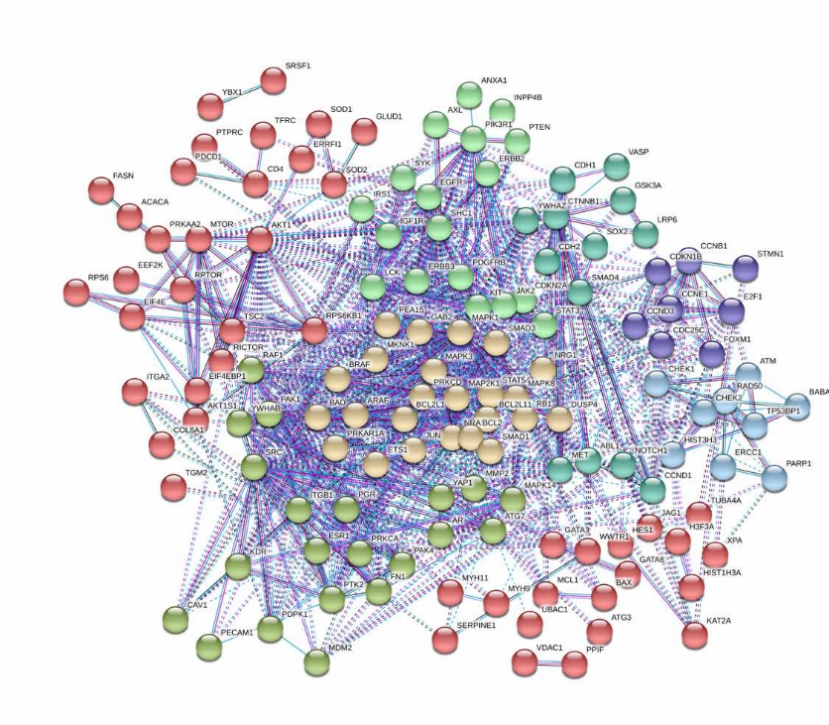
该文是RPPA蛋白组学领域的开山大作,阐明了RPPA技术能够提升多组学整合性分析的潜力,是一种功能强大的系统蛋白组学分析方法,随之被应用多个TCGA泛癌项目中,开辟了一个新的蛋白组学应用场景,并且已被广泛应用于研究肿瘤起始/进展及生物标志物开发和药物机制研究。RPPA技术作为一种开源的技术,根据需求可以实现几十种至几百种蛋白质靶点及翻译后修饰靶点的丰富分析,而主要应用方向则涵盖了关键的癌症信号通路及转导途径(如图8)。
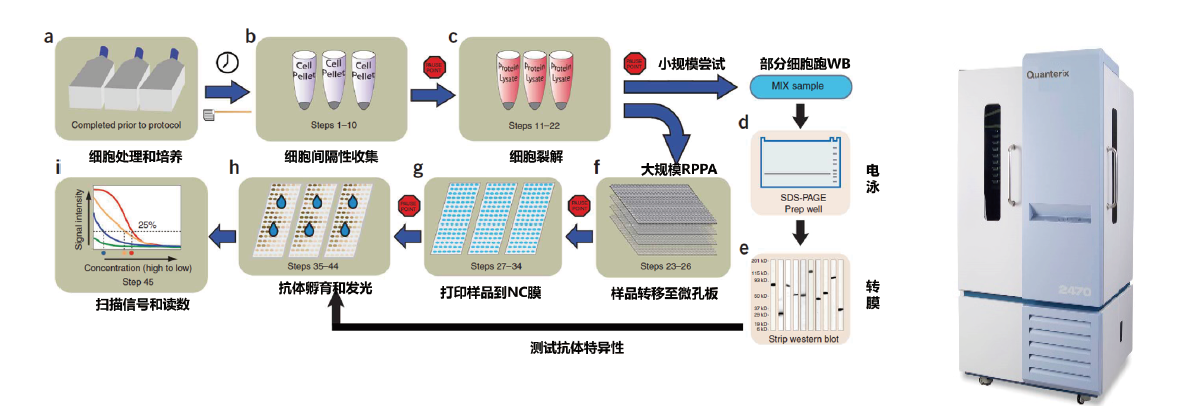
杭州纽蓝科技有限公司是一家实验室科学仪器及技术综合解决方案供应商,专注于医学、和制药领域,同时拥有自主研发的NeoSPR无标记分子互作产品及检测服务。纽蓝科技旨在推动RPPA技术在国内的应用和发展。纽蓝科技代理美国Quanterix公司的全球首款实心针高通量微阵列打印仪2470Arrayer在中国区的销售的技术支持。2470 Arrayer的实心针打印方式实现了对细胞或组织裂解液等粘稠度很高的样品即快速又精确的打印,已经帮助MD 安德森癌症中心、德国癌症中心、神奈川癌症中心、芬兰癌症中心、乔治梅森大学、贝勒医学院等机构搭建了RPPA技术平台并得到了广泛的使用,发表了300余篇高水平的期刊。
扫描下方二维码或注册链接进行报名,报名成功后从收到的邮件中点击链接登录

注册链接:https://quanterix.zoom.us/webinar/register/WN_QpRfaZilRuKd4AMGcIJ19A
如需研讨会PPT和其他RPPA技术资料请扫描下方二维码

如欲了解更多相关信息,请联系
杭州纽蓝科技有限公司地址:浙江省杭州市余杭区良渚街道金昌路2073号汇盈产业园3号楼5层
电话:+86-0571-868002717、+86-18667018195
邮箱:fwmeng@nl17.com
网址:www.nl17.com 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发