潘跃银教授:正确认识肿瘤免疫治疗的获益
| 导读 | 和假性进展。既然肿瘤免疫治疗独特,那我们如果用“旧”的观念来评价它,是不是不太合适呢?而我们又该如何更好地转变“老”观念来适应新变化呢? |
潘跃银 教授
主任医师,教授,博士生导师
安徽省肿瘤医院副院长
中科大附一院肿瘤教研室主任
安徽省肿瘤质量控制中心副主任(兼)
合肥离子医学中心副主任(兼)
中国临床肿瘤协会(CSCO)理事
安徽省医学会乳腺病分会候任主任委员
安徽临床肿瘤学会候任理事长
安徽省抗癌协会副理事长
中国抗癌协会乳腺癌专业委员会委员
中国临床肿瘤协会乳腺癌、免疫、肝癌、肾癌专家委员会委员
中国临床肿瘤协会肿瘤预防专业委员会委员
中国医促会姑息与人文关怀专业委员会常委
中国医促会胸部肿瘤专业委员会委员
《临床肿瘤学杂志》、《Journal Thoracic Oncology》、《中华医学杂志》等编委
潘教授您好,请问您认为,与传统治疗相比,肿瘤免疫治疗在临床获益上的优势有哪些?
潘跃银教授:与传统的治疗不同,肿瘤免疫治疗能给患者带来长期的生存获益和持久的免疫应答,即使对于SD的患者,也能带来持续的生存获益,比如许多肿瘤免疫治疗临床试验的生存曲线都会出现一个“长尾”效应,而且未出现进展的患者疗效维持的时间也很长。
长期生存,就是既往晚期非小细胞肺癌在化疗时代生存的时间是有限的,在二线治疗当中,它的有效率大约是9%左右,中位的OS大概只有6个月左右,生存时间非常有限。来自美国SEER数据库的资料显示,晚期非小细胞肺癌在化疗时代,它的5年生存率不足5%。
以PD-1和PD-L1抑制剂为代表的、针对免疫检查点的肿瘤免疫治疗,显著改善了晚期非小细胞肺癌患者的长期生存。目前,肺癌肿瘤免疫治疗随访时间最长的生存数据来自于纳武利尤单抗的CheckMate 003(CA209-003)研究,它的5年随访结果显示,纳武利尤单抗单药治疗二线以及以后的非小细胞肺癌患者,5年生存率达到了16%,相对传统的化学治疗提高了3倍。
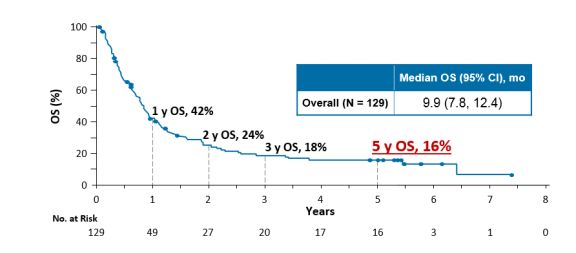
CA209-003研究中,使用纳武利尤单抗后的OS获益
纳武利尤单抗全球Ⅲ期肺癌注册临床研究CheckMate 017和057的3年随访结果显示,鳞癌和非鳞癌的晚期非小细胞肺癌患者二线使用纳武利尤单抗单药治疗,3年的生存率分别可以达到16%和18%,与多西他赛相比,免疫检查点抑制剂单药治疗大大降低了肺癌患者的死亡风险,使得这些患者从治疗中真正获得了生存获益,达到了长期的生存,这在过去的化疗时代是不可想象的。
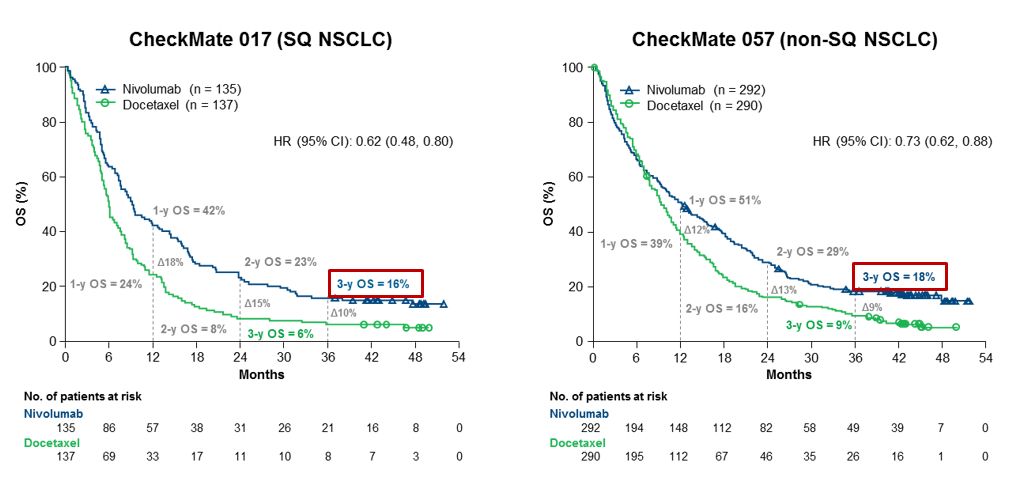
CheckMate017和CheckMate057研究中,使用纳武利尤单抗后的OS获益
而首个来自于我们中国人自己的Ⅲ期免疫治疗的临床研究,CheckMate 078也显示,纳武利尤单抗中位的OS达到了12个月,相较于多西他赛,死亡风险下降了32%。而另一个Ⅰ期临床研究,Keynote 001研究显示,PD-1抑制剂pembrolizumab与多西他赛相比,可以提高经治的非小细胞肺癌患者的3年生存率。
第二个,就是持续应答。癌症的临床治疗有这样一个特点:在治疗方案上,越靠后的治疗方案可能起效的可能性越低,起效的持续时间也越短。观察免疫治疗的疗效不但要看有效率,也应该关注疗效的持续时间,也就是所谓的应答时间(DOR, duration of response)的概念。CheckMate 003和Keynote 010的研究均表明,PD-1抑制剂治疗2年后停药,大部分患者仍可持续应答。Ⅲ期的临床研究CheckMate 017中,纳武利尤单抗二线治疗鳞状的非小细胞肺癌患者的DOR为25.2个月,而且随访3年时,26%的患者仍然在持续的缓解中。在CheckMate 057中,随着随访时间的延长,纳武利尤单抗二线治疗非鳞非小细胞肺癌患者中的DOR达到了17.2个月,而且随访3年时达到了18.3个月,仍有23%的患者产生持续的效应。

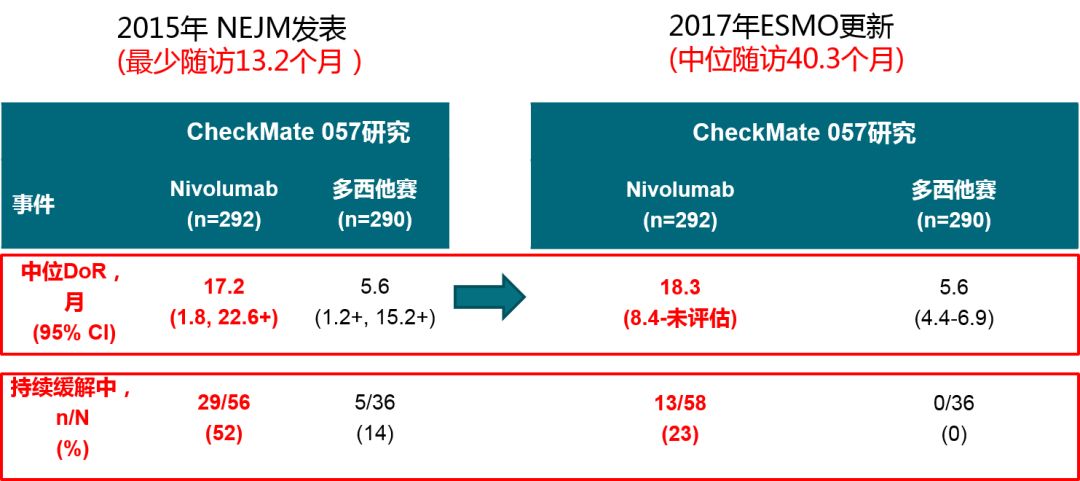
CheckMate 017/057研究中,部分3年存活患者仍在持续应答
CA209-003研究是随访时间最长的一个免疫检查点抑制剂的试验,5年随访时有75%的仍存活患者在纳武利尤单抗治疗之后没有接触过任何治疗,但是在末次随访时,仍然没有出现疾病的进展。
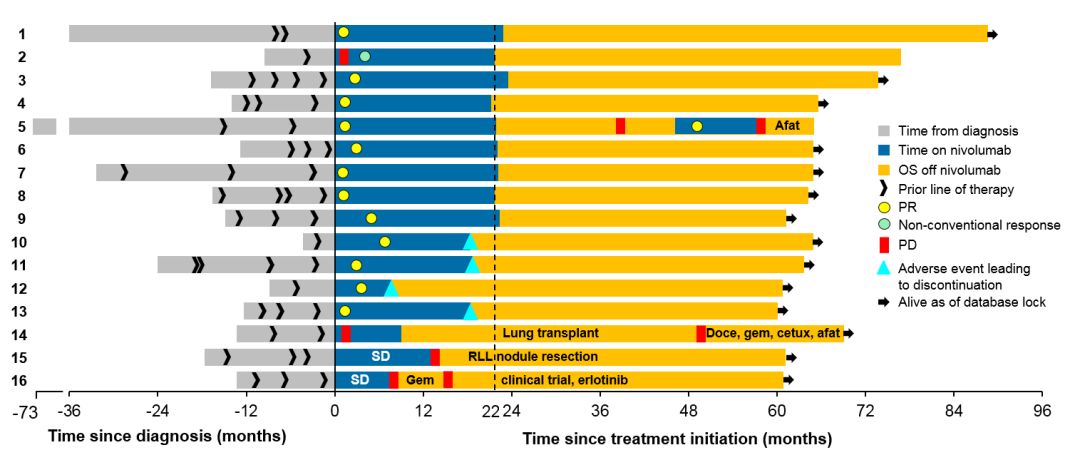
CA209-003研究中,75%的5年存活患者仍在持续应答
这种肿瘤对肿瘤免疫治疗长期应答的现象在其他癌症的研究中也被观察到,比如纳武利尤单抗联合ipilimumab治疗恶性黑色素瘤的CheckMate 069研究表明,即使患者由于毒性反应等原因而终止用药,治疗的反应仍可持续一段时间。美国的一个研究团队曾经对多个中心的应用PD-1和PD-L1抑制剂治疗有效,却因免疫治疗相关的毒副反应而停药的转移性肾细胞癌的患者进行回顾性分析,发现中位用药时间为9个月的患者,PD-1和PD-L1抑制剂停药以后,仍然获得了中位22个月的无进展生存。
既然肿瘤免疫治疗有这些与传统治疗不同的特征,那您觉得传统的临床终点是否还适用于肿瘤免疫治疗?
潘跃银教授:一般来说在Ⅱ期临床试验中,评估新的抗癌药物的初步疗效通常使用客观缓解率(ORR)作为主要的临床试验终点。这些药物主要在单臂的试验中进行检测,并根据历史对照数据来预测是否达到预期ORR的改善,以确定是否开展Ⅲ期的随机对照的临床试验。采用这种方法监管机构也更有可能对ORR高的药物给予初步的审批。
传统的临床试验终点依赖在不同的药物剂量下对肿瘤大小的评估,假设肿瘤体积的变化趋势是单一的,那么化疗药物的效应发挥迅速,在首次化疗给药的几周后都会出现明显的肿瘤应答,但肿瘤免疫治疗与肿瘤化疗药物的作用机制完全不同,在免疫检查点单抗的临床试验中,有一部分病人的肿瘤体积在前几个月会变大,肿瘤药物的疗效要几个月以后才会逐渐的显现,然后肿瘤体积再逐渐的变小,得到控制。这也就是按照RECIST的1.1的标准,以评定为PD的患者继续治疗以后病灶会再度缩小。所以用RECIST的标准来评价可能是不合适的。
接受化疗疗效评估为SD的患者临床获益是比较有限的,但是越来越多的临床资料显示,肿瘤免疫治疗以后,长期SD也可以看作是药物起效的一种表现,比如在CheckMate 017和057的研究随访中发现,治疗后评估SD的这些患者,其死亡的风险较多西他赛组仍然可以降低40%左右,有明显的生存获益。
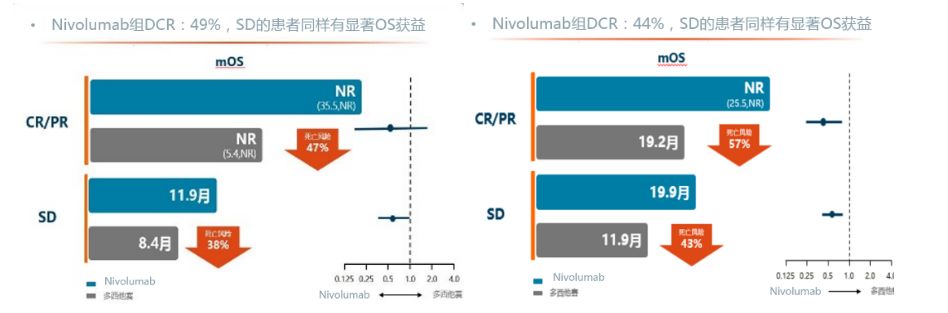
肿瘤免疫治疗SD的患者也可有生存获益
所以,传统的临床终点(如RECIST确定的ORR、PFS)可能无法完全反映免疫治疗的临床获益,如抗PD-1以及抗PD-L1抗体与多西他赛的头对头比较中,肿瘤免疫治疗的总有效率仅为15%-20%,PFS似乎也没有明显的改善,但是患者总生存期却显著的延长。肿瘤疗效评估的金标准是OS,免疫治疗最显著的特征是患者的长期生存,因此单看ORR、PFS可能是较为局限的。
针对上面的问题,您认为导致传统临床终点可能不适宜肿瘤免疫治疗的原因是什么?
潘跃银教授:肿瘤的免疫治疗与传统治疗的作用机制不同,传统的治疗比如化学治疗是直接作用于肿瘤细胞本身,而肿瘤免疫治疗是作用于人体的免疫系统,诱导患者去调节机体对肿瘤的免疫应答,比如PD-1和PD-L1抑制剂,它是通过阻断PD-1和PD-L1的结合,解除免疫检查点通路对T细胞的活化,识别肿瘤细胞的抑制作用,重启T细胞对肿瘤细胞的免疫杀伤作用,那么这种独特的作用机制使得免疫治疗产生了不同于传统治疗的非常规的应答模式,也就是延迟反应和假性进展。
第一个是延迟反应,如果分析治疗反应与治疗时间的关系,与化疗和靶向药物相比,PD-1和PD-L1抗体治疗后的部分患者的肿瘤变化相对比较缓慢,称为延迟反应。与传统的治疗不同,肿瘤免疫治疗是作用于自身的免疫系统,免疫细胞的活化、增殖,从而启动肿瘤细胞的免疫,这个过程需要数周时间,因此相对于传统的治疗方法,PD-1抑制剂免疫治疗的起效时间一般在2-3个月(8-12周)左右,因此建议在该时间段进行影像学的检查,提高肿瘤治疗的评估性。
第二个是假性进展,是指治疗的初期,病灶在影像学上显示为增大,按照传统的疗效评价标准判定为PD,但是患者的体力状态和临床症状并没有出现明显的恶化,继续治疗以后会出现肿瘤缩小的这种现象。肿瘤免疫治疗通过调节T细胞的功能激活免疫系统,影像学检查观察到肿瘤阴影面积的增大,实际上是免疫细胞向肿瘤病灶聚集与浸润的表现,越多的免疫细胞进入肿瘤的病灶区域,意味着肿瘤细胞被杀死的概率越大。所以,这种情况不一定是由于治疗无效,而可能是产生治疗效果的一种表现。而irRECIST标准2017版也对肿瘤免疫治疗的疾病进展评估标准做了详细的描述,建议在第一次影像学进展后的4-8周再次进行PD的确认。
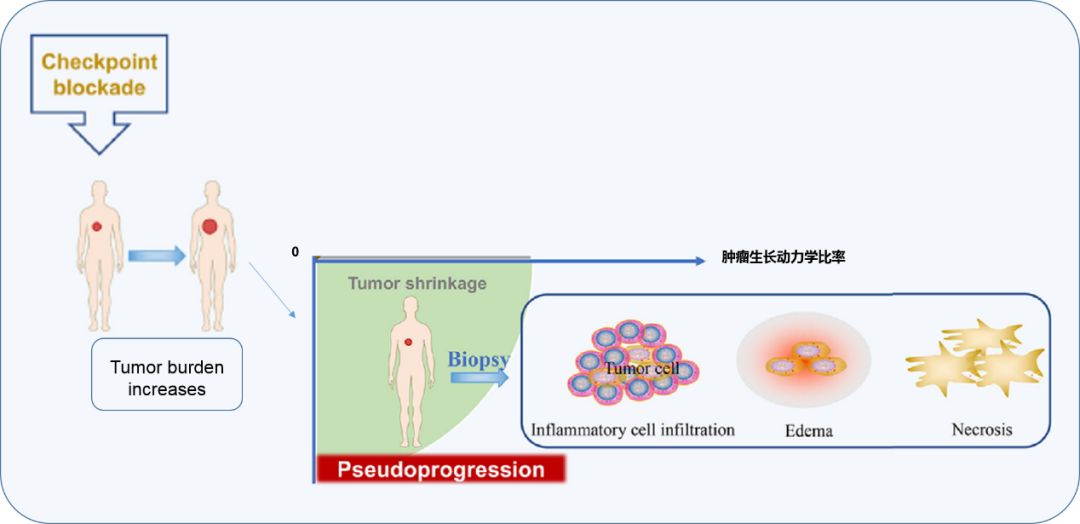
肿瘤免疫治疗的特征之一:假性进展
最后,能否请您介绍一下,我们在临床中如何能更好地评价肿瘤免疫治疗的临床获益?
潘跃银教授: ORR和PFS作为肿瘤治疗的短期疗效评价指标具有一定的局限性,在涉及到免疫检查点抑制剂的临床研究中,ORR不能准确的反映患者的生存期,而基于肿瘤免疫治疗假性进展的存在,PFS可能也不能准确的反应患者的疗效获益。因此,结合肿瘤免疫治疗长期生存和持久获益的治疗特征,肿瘤免疫治疗的疗效评估更需要结合OS和DOR的综合进行考量,目前有专家提出了可以观察到某一个时间点(如1年,2年或3年)的生存率作为肿瘤免疫治疗临床试验的终点指标,也就是里程碑的分析。
这一分析方法有诸多的优点,如简单,可以克服生存曲线中位时间延迟的缺点等。统计学分析表明,较短的时间节点分析与长期生存的相关性较差,如9个月的PFS率或6个月的ORR率,同OS HR之间未见相关性,而12个月的OS率与OS HR之间存在着中等程度的相关性。
因此,治疗某段时间后的OS率可能成为肿瘤免疫治疗总生存获益的预判指标之一,但是选择12个月还是9个月的OS率作为临床的研究终点,仍需要开展更多临床试验进一步来探讨。综合分析,肿瘤免疫治疗的疗效评价更应该结合肿瘤免疫治疗特征来做综合的评估,更加的合理。(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发