CFDA重磅!晚期乳腺癌患者迎来首款CDK4/6抑制剂获批上市!
| 导读 | 辉瑞制药公司宣布,CFDA正式批准了首个CDK4/6抑制剂爱博新(哌柏西利)的中国上市申请.用于一线联合芳香化酶抑制剂治疗绝... |
乳腺癌作为女性发病率排名第一的恶性肿瘤,呈逐年高发趋势。约有60%-70%的乳腺癌是激素受体阳性(HR+)的,适用内分泌治疗。
影像学显示的乳腺癌细胞
与化疗相比,内分泌治疗不良反应小,使用方便,是HR+晚期乳腺癌治疗的首选。
但是,内分泌治疗最终可能导致耐药,因此内分泌药物的联合治疗已经成为一种趋势,而氟维司群或来曲唑联合CDK4/6抑制剂方案更是成为一种颇具前景的内分泌治疗新选择。
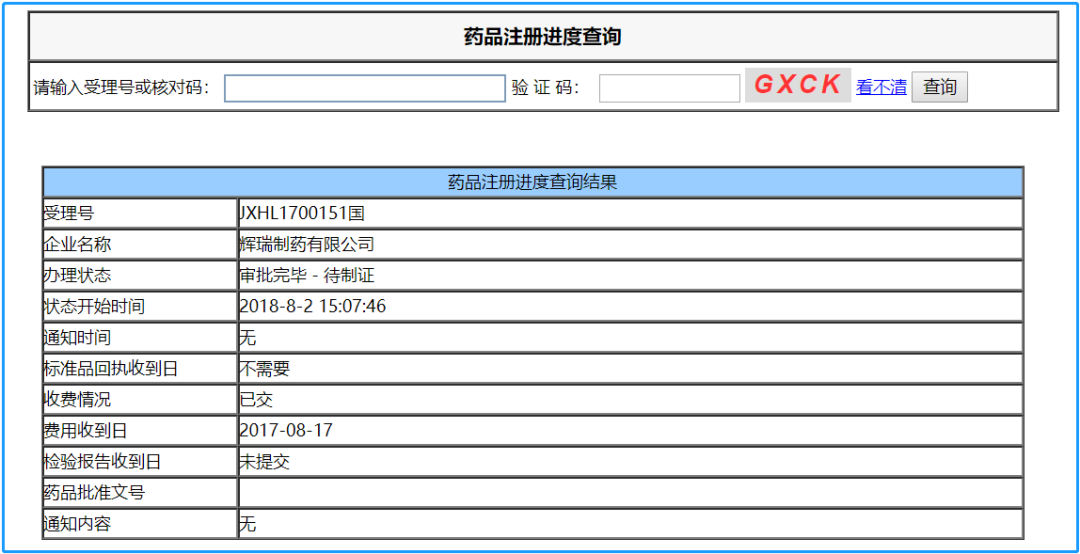
今天!终于!辉瑞制药公司宣布,CFDA正式批准了首个CDK4/6抑制剂爱博新(哌柏西利)的中国上市申请。用于一线联合芳香化酶抑制剂治疗绝经后女性,激素受体阳性(HR+)、HER2-局部晚期或转移性乳腺癌。成为全球第87个获得批准的国家!
激素受体阳性(HR+)包括ER+(雌激素受体阳性)和/或PR+(孕激素受体阳性),内分泌治疗是激素受体阳性乳腺癌的主要治疗手段,内分泌耐药是这部分患者肿瘤复发或进展的主要原因,而CDK4/6抑制剂带来了新的治疗可能。
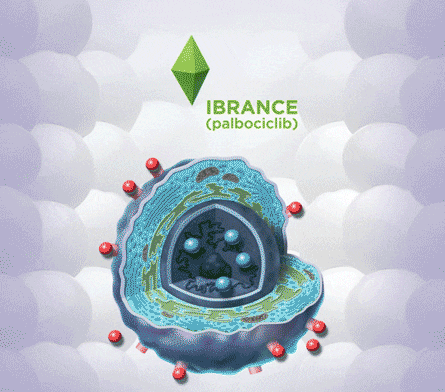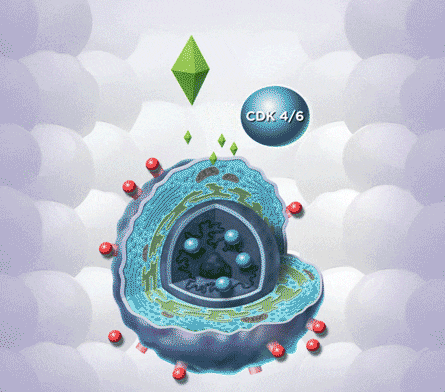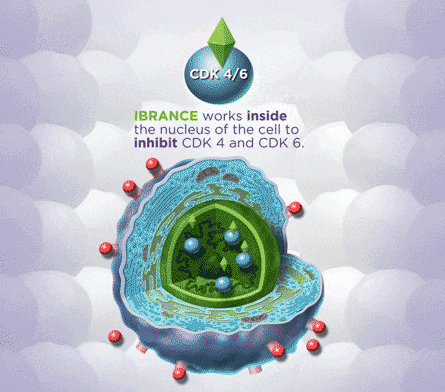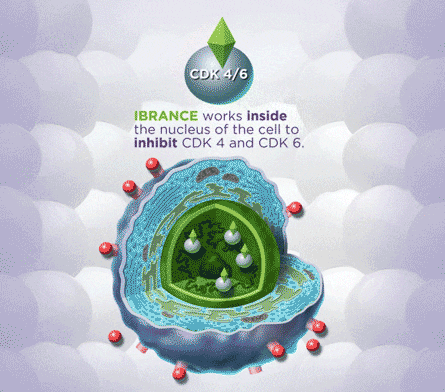
CDK4/6抑制剂作用机制
爱博新是全球首个成功获批上市的CDK4/6抑制剂,最先获得美国FDA批准(2015年2月3日)。截至目前,爱博新已在全球86个国家和地区获批上市,中国是第87个。

在爱博新全球注册研究PALOMA-1中,一线治疗为来曲唑联合爱博新对比来曲唑单药,其无进展生存期由10.2个月延长至20.2个月。得益于该研究的突破性进展,爱博新获得FDA的快速审批通道。
在后续补充验证性Ⅲ期试验PALOMA-2中,扩大样本量的最终研究结果提示:中位PFS时间联合治疗组高达24.8个月,单药来曲唑组为14.5个月。爱博新联合治疗显著延长患者无进展生存期,并且显著降低死亡风险。
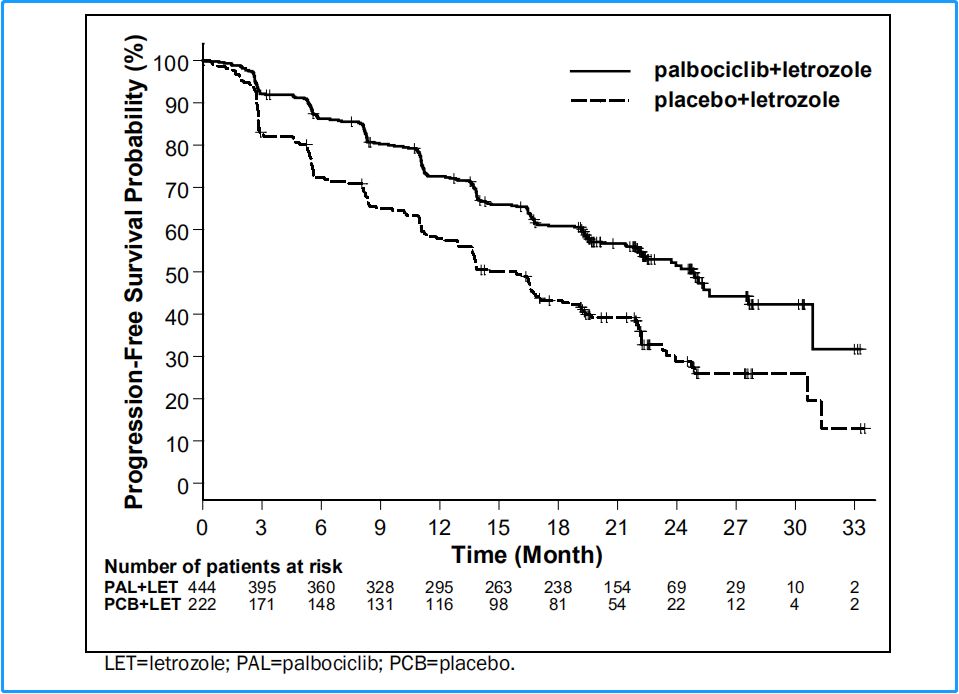
国内此次批准适应证为爱博新联合芳香化酶抑制剂,如:来曲唑、阿那曲唑、依西美坦,作为HR+、HER2-的绝经后晚期乳腺癌患者的初始内分泌治疗。
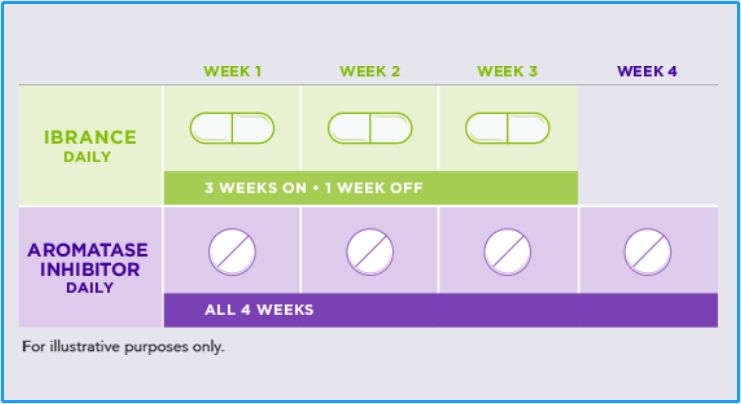
爱博新联合芳香酶抑制剂使用方法:
爱博新和芳香酶抑制剂用药每4周一个周期,前三周每日使用一次爱博新和一次芳香酶抑制剂,第四周只用芳香酶抑制剂,不用爱博新,4周结束后重新开始。
爱博新的获批上市,对国内激素受体阳性的乳腺癌患者来说,是真正的好消息!
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发