阿斯利康Ⅲ期甲状腺癌临床试验失败 | 信达生物两款单抗新药同时获...
| 导读 | 阿斯利康(AstraZeneca)其MEK 1/2抑制剂司美替尼(selumetinib)治疗甲状腺癌的Ⅲ期临床试验(ASTRA)因未达研究主要终点而宣告失败,并将终止该适应症开发。 |
阿斯利康Ⅲ期甲状腺癌临床试验失败。阿斯利康(AstraZeneca)其MEK 1/2抑制剂司美替尼(selumetinib)治疗甲状腺癌的Ⅲ期临床试验(ASTRA)因未达研究主要终点而宣告失败,并将终止该适应症开发。先前司美替尼用于晚期甲状腺癌的中期研究结果显示,该药针对碘难治性分化型甲状腺癌患者的碘摄取和保留显示“临床上有意义的提高”。目前,该药于1型多发性神经纤维瘤的Ⅲ期临床试验,以及与其他药联合的多项临床试验仍在进行。
国内药讯
1. 临床试验申请“60天”默许制正式落地。国家药监局发布公告,对药物临床试验审评审批的有关事项作出调整:在我国申报药物临床试验的,自申请受理并缴费之日起60日内,申请人未收到国家食品药品监督管理总局药品审评中心(药审中心)否定或质疑意见的,可按照提交的方案开展药物临床试验。
2. 国家药监局回应华海药业缬沙坦原料药有关情况。7月29日,针对华海药业缬沙坦原料药中检出微量N-亚硝基二甲胺(NDMA)杂质有关情况,国家药监局新闻发言人介绍,对所有国内在产的7家缬沙坦原料药生产企业(含华海药业)进行风险排查,除华海药业缬沙坦原料药NDMA杂质超出限值外,其他国内缬沙坦原料药生产企业,NDMA杂质检出值低于限值或者未检出。同时提醒,正在服用缬沙坦药品的患者一定不要擅自停药,擅自停药对于高血压患者的风险更直接且严重。
3. 信达生物两款单抗新药同时获临床试验批件。信达生宣布其注射用重组全人源抗OX40单克隆抗体(IBI101)和重组全人源抗RANKL单克隆抗体注射液(IBI307)同时获得国家药监局核准签发的《药物临床试验批件》。其中,注射用重组全人源抗OX40单克隆抗体是一种OX40激动剂,拟用于治疗多种肿瘤疾病。而重组全人源抗RANKL单克隆抗体拟用于治疗骨质疏松和与癌症转移相关的溶解性骨损害。
4. 百济神州公布在港股票发行计划。7月27日,百济神州公布计划通过香港首次公开发行及全球股票发行65,600,000股普通股,发行股票计划在香港联合交易所有限公司主板上市。据悉,募集资金将用于透过内部研究及外部授权及业务发展合作,为在癌症及其他潜在治疗领域的产品组合持续扩充提供资金(包括内部早期临床及临床前阶段的在研制剂及已获许可的在研制剂开发成本)等。
5. 勃林格殷格翰慢阻肺新药在中国获批上市。勃林格殷格翰(Boehringer-Ingelheim)宣布,思合华®能倍乐®(噻托溴铵/奥达特罗吸入喷雾剂)获得国家药监局正式批准上市,用于慢性阻塞性肺疾病(包括慢性支气管炎和肺气肿)患者的长期维持治疗。在全球共纳入超过15,000例慢阻肺患者的 III期临床研究结果显示,思合华®能倍乐®较噻托溴铵喷雾剂进一步改善慢阻肺的主要临床指标(包括肺功能、呼吸困难等),且安全性与单药治疗相当。
6. 科伦药业KL280006注射液获临床试验批件。科伦药业宣布其开发的创新镇痛药物外周κ受体激动剂 KL280006 注射液(规格: 1mL:0.1mg; 10mL:2mg)获国家药监局核准签发的《药物临床试验批件》,拟用于治疗急性疼痛(如术后疼痛)。非临床研究数据证实 ,KL280006 注射液对外周κ 受体具有高亲和性和高选择性,不易透过血脑屏障,镇痛效果确切,兼具良好的安全性和耐受性。目前,全球尚无外周选择性κ 受体激动剂类药物获批上市。
7. 成都先导与赛诺菲签订DNA编码化合物库筛选协议。成都先导宣布与赛诺菲(Sanofi)达成一项DNA编码化合物库筛选协议,以期发现新颖的小分子化合物用于新药研发。基于此协议,成都先导将充分利用在DNA编码化合物库设计、合成及筛选方面的先进技术平台和研发能力为赛诺菲关注的多个治疗靶点进行筛选。筛选出的先导化合物将排他性地转让给赛诺菲,并同时支付成都先导首付款及后续里程碑款。具体金额未被批露。
8. 同润生物医药获1.5亿美元A轮融资。同润生物医药宣布完成1.5亿美元A轮融资,由通和毓承、博裕资本以及淡马锡共同投资。同润生物医药致力于研发下一代肿瘤免疫治疗药物,其研发管线中拥有数个具有竞争力的全新肿瘤免疫治疗分子。此轮融资将用于推动其研发管线中分子的临床前开发和临床试验,以及进一步拓展公司现有产品管线。
国际药讯
1. GSK的COPD抗炎药新适应症遭PADAC拒绝。葛兰素史克(GSK)公司宣布,其抗炎药Nucala(mepolizumab,美泊利单抗)作为吸入性皮质类固醇维持方案的附加疗法治疗嗜酸性粒细胞性慢性阻塞性肺病(COPD)的新适应症申请遭FDA肺变态反应药物咨询委员会(PADAC)拒绝。PADAC认为,Nucala的风险效益不足以支持其批准。而这与不久前FDA内部审查员给出的结论一致。Nucala是全球首个靶向IL-5的生物疗法,于2015年获FDA批准治疗重度嗜酸性粒细胞哮喘,并于2017年获FDA批准治疗嗜酸性肉芽肿血管炎(EGPA)。
2. AC Immune阿尔茨海默病单抗药Ⅱ期临床结果积极。瑞士AC Immune公布其全人源的IgG 4单克隆抗体crenezumab在98例罹患中重度阿尔茨海默病的患者Ⅱ期临床试验ABBY及BLAZE的研究数据。结果显示, Crenezumab治疗与脑脊液中β-淀粉样蛋白质(Abeta)低聚体水平的持续下降相关联;86%的静脉注射患者和89%的皮下注射患者,在69周时的淀粉样蛋白低聚体低于基线水平(相较安慰剂,静脉注射p<0.001/皮下注射p<0.001)。
3. 基因泰克眼植入物治疗AMD Ⅱ期临床结果积极。罗氏(Roche)旗下基因泰克(Genentech )公司公布一项Ⅱ期临床LADDER研究的积极结果。该研究旨在评估其新型给药系统ranibizumab PDS(雷尼单抗玻璃体植入物)在湿性年龄相关黄斑变性(AMD)患者中的安全有效性。结果显示,超过半数的患者在第一次PDS植入装置与需要再次填充药物之间经过了6个月或更久的时间,且大剂量PDS组的视力结果与每月的ranibizumab眼注射结果相似,并在整个研究期间保持不变。
4. Nabriva收购一潜在first-in-class抗生素新药。Nabriva Therapeutics宣布收购Zavante Therapeutics及其在研抗生素CONTEPO™。根据双方协议条款,Nabriva将向Zavante支付820万股的预付款,以及后期可能高达9750万美元的里程碑付款。CONTEPO™(注射用磷霉素,曾用名为ZTI-01和ZOLYD)是一种新型、潜在first-in-class的在研静脉注射(IV)抗生素,已被FDA授予快速通道资格,用于治疗复杂性尿路感染(cUTIs)等。Nabriva预计将于今年第四季度向FDA提交CONTEPO™的新药申请(NDA)。
5. Alector获1.33亿美元E轮融资。美国Alector公司宣布获得1.33亿美元E轮融资,用于推进其临床计划,并扩展其免疫神经学(immuno-neurology)研发平台。该平台力图开发靶向小胶质细胞(microglia,中枢神经系统中的免疫细胞)表面受体蛋白的单克隆抗体,以调节阿兹海默病(AD)患者大脑中免疫细胞的功能,从而在更有效地清除淀粉样蛋白沉积的同时,不会引起大规模的炎症反应。目前,其在研药物AL002和AL003分别靶向大脑中的免疫系统受体TREM2和SIGLEC-3。
医药热点
1. 证监会修改退市政策:涉公众健康安全领域重大违法的应退市。27日晚间,中国证监会发布《关于修改的决定》,对2014年《关于改革完善并严格实施上市公司退市制度的若干意见》(简称《退市意见》)进行修改,明确上市公司涉及到公共安全、生态安全、生产安全和公众健康安全等领域的重大违法行为的,证券交易所应当严格依法作出暂停、终止公司股票上市交易决定。《决定》自2018 年7 月27 日起施行。
2. 国务院调查组已基本查清长生生物的违法事实。据国务院调查组消息,长春长生公司违法违规生产狂犬病疫苗案件调查工作取得重大进展,已基本查清企业违法违规生产狂犬病疫苗的事实。该企业为降低成本、提高狂犬病疫苗生产成功率,违反批准的生产工艺组织生产,包括使用不同批次原液勾兑进行产品分装,对原液勾兑后进行二次浓缩和纯化处理等,且为掩盖上述违法违规行为,企业有系统地编造生产、检验记录,开具填写虚假日期的小鼠购买发票,以应付监管部门检查。
3. 长春长生董事长高俊芳等18人被提请批捕。7月29日,依据《中华人民共和国刑事诉讼法》第79条规定,长春新区公安分局以涉嫌生产、销售劣药罪,对长春长生生物科技有限责任公司董事长高某芳等18名犯罪嫌疑人向检察机关提请批准逮捕。目前,案件审理工作正在进行中。
4. 总经费2.03亿!一批国家重点研发计划项目出炉。中国生物技术发展中心公示国家重点研发计划“重大慢性非传染性疾病防控研究”重点专项2018年度定向项目拟立项清单,拟立项项目总数共10个,总经费达到2.03亿元。其中,中国医学科学院肿瘤医院牵头的“恶性肿瘤规范化早诊早治关键技术集成及应用体系建设研究 ”项目,总经费更是多达4862万元。
5. 国内唯一一家干细胞医院在海南博鳌乐城先行区落成。中国干细胞集团在博鳌乐城国际医疗旅游先行区建成中国干细胞集团海南博鳌附属干细胞医院。作为国内唯一一家干细胞医院,该医院致力于打造成为全国具有影响力的血液病治疗平台,定位于“大专科、小综合”专科医院,设有100个百级无菌层流病房,每年可完成造血干细胞移植超过1000例,是全国规模最大的干细胞医院,将有效缓解国内白血病患者移植资源紧张的困境。
股市资讯
上个交易日 A 股医药板块 -0.48%
涨幅前三 跌幅前三
沃森生物 +10.00% 海利生物 -10.00%
嘉应制药 +9.94% 通化东宝 -9.81%
永安药业 +6.84% 四环生物 -5.68%
【科伦药业】1)控股子公司博泰生物开发的创新镇痛药物外周κ受体激动剂KL280006注射液获国家药监局核准签发的《药物临床试验批件》;2)与兴业租赁签署了《融资租赁合同》,以公司及子(分)公司名下固定资产以售后回租的方式进行融资租赁交易,融资金额3亿元,租赁期限3年。
【九强生物】一种磁微粒化学发光试剂的制备方法获得专利证书。
【美康生物】小而密低密度脂蛋白胆固醇检测试剂盒(过氧化物酶法)取得医疗器械注册证。
【开立医疗】全自动血液细胞分析仪完成第二类医疗器械注册证核发并取得了《中华人民共和国医疗器械注册证》。
【广生堂】收到CFDA下发的关于公司恩替卡韦胶囊一致性评价的受理通知书。
审评动向
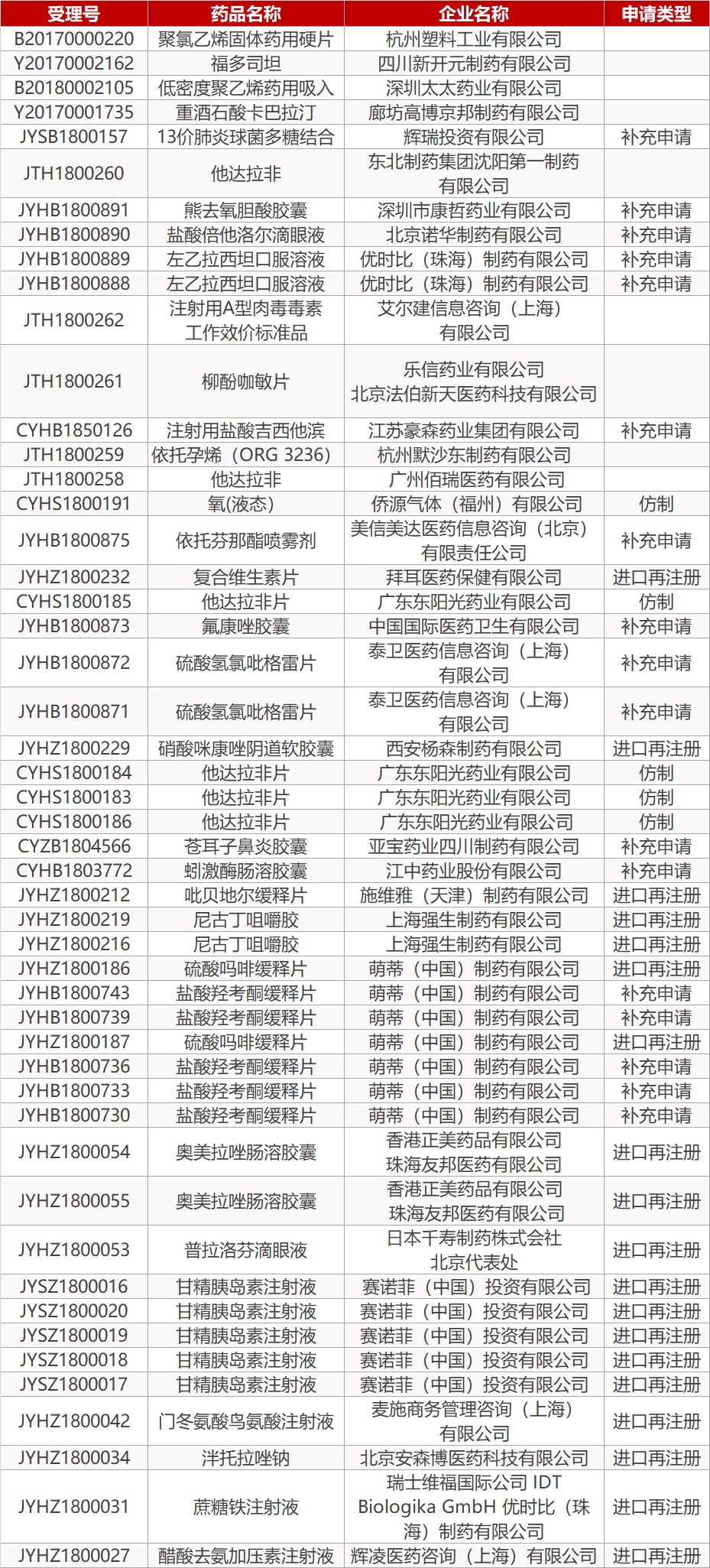
1. CDE最新受理情况(7月27日)
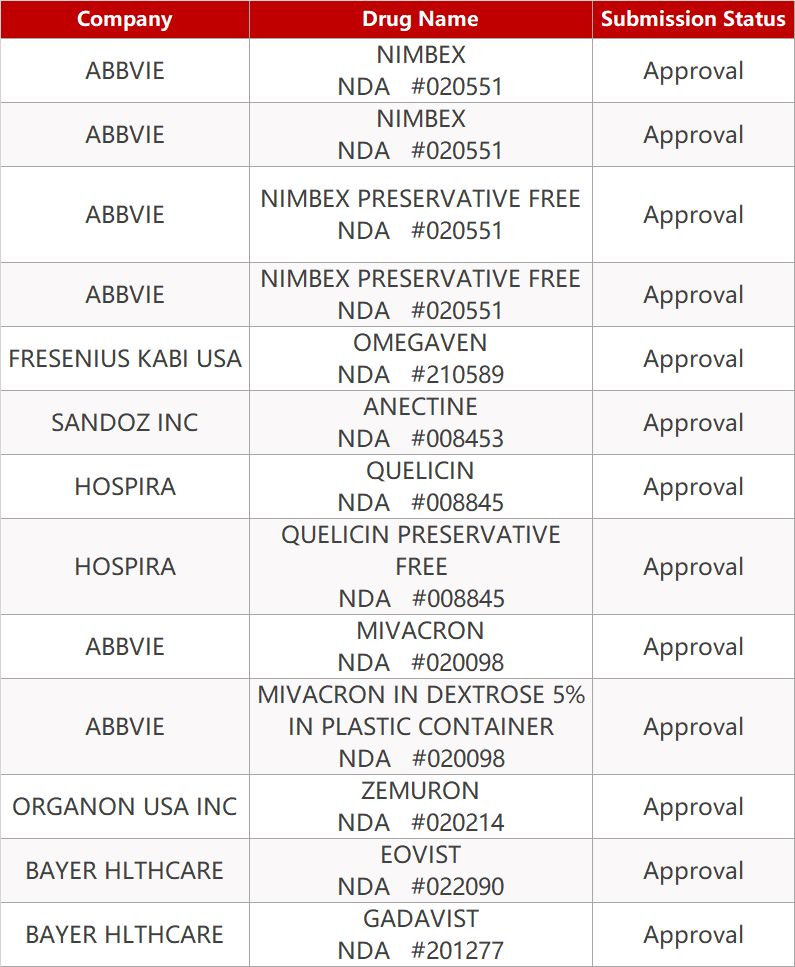
2. FDA最新获批情况(北美7月26-27日)
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发