全力推进基因疗法,FDA发布6大新指南
| 导读 | 近日,美国FDA局长ScottGottlieb博士发表声明,宣布FDA将继续大力推进基因疗法的开发,并发布了6大新指南。 |
近日,美国FDA局长Scott Gottlieb博士发表声明,宣布FDA将继续大力推进基因疗法的开发,并发布了6大新指南。在今天的这篇文章中,药明康德微信团队也将为各位读者整理分享新指南的具体内容。
基因疗法曾经只是一种理论,现在对于患者来说已经成为一种治疗现实。基因疗法具有治疗和治愈一些难治性的疾病的潜力。FDA为基因产品如何开发、监管机构审核和报销建立的政策框架,将有助于为这个新市场的持续发展奠定基础。去年,我们发布了再生医学框架草案,提到了加速开发的几种途径,例如突破性疗法认定和再生医学先进疗法认定(RMAT),这些可能适用于基因疗法的开发机构。今天,FDA为基因疗法的开发、审查和批准推出一个补充框架。

▲2017年11月发布的再生医学框架草案中,FDA提到将采取5种途径加快再生医学产品审批(图片来源:FDA官网)
在过去的12个月中,FDA批准了三种基因疗法产品。这反映了该领域的快速发展。我们达到了一个拐点,能够可靠地将基因盒(gene cassettes)输送到体内、细胞和人体中。未来,我们预计该领域将继续向前发展,可能会有许多治疗衰弱性疾病的基因疗法获批。这些疗法有很大的希望。我们的新举措旨在促进这一创新领域的发展。
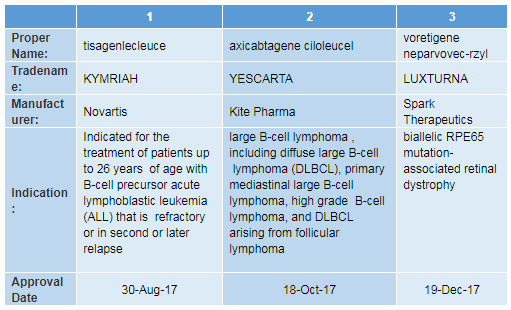
▲FDA批准的3种基因疗法(信息来源:FDA官网)
基因疗法正在针对许多疾病领域进行研究,包括遗传疾病,自身免疫疾病,心脏病,癌症和艾滋病。我们期待与学术界和研究界合作,为更多患者提供安全有效的产品。但我们知道,我们仍然需要了解基因产品的工作原理,如何安全地使用它们,以及它们是否能够在体内继续正常工作而不会产生长期副作用。与传统的药物审查相比,基因治疗更具挑战性的问题是产品制造和质量,或者是反应持久性,这在任何合理规模的上市前试验中往往无法完全回答。在批准一些基因产品时,我们可能需要接受这些问题在某种程度上的不确定性。例如,在某些情况下,在批准时还不知道是否长期有效。进行可靠的上市后跟踪的有效工具,例如所需的上市后临床试验,将成为推动基因治疗领域发展的关键,并帮助确保能够带来安全和创新的疗法。
即使可能存在不确定性,我们也需要确保患者安全,并充分描述基因产品的潜在风险并证明其有益。基因产品最初的目的是治疗毁灭性疾病,其中许多缺乏治疗方法,包括一些致命性疾病。在没有可用疗法的情况下,FDA历来愿意接受更多的不确定性,以便及时获得有希望的疗法。在这种情况下,药物申办方通常需要进行上市后临床试验,称为4期临床试验,以确认药物的临床益处。这是国会给予FDA的权力,例如实施加速批准这样的路径。
当涉及基因治疗等新技术时,FDA将与时俱进,以确保适应这些新技术平台所带来的独特挑战。今天,我们正在朝着塑造现代基因疗法监管结构方面迈出一步。FDA计划发布一套六个科学指导文件,作为全面监管框架的基石,帮助我们推进基因治疗领域,同时确保新产品符合FDA的安全性和有效性黄金标准。
3个特定疾病基因治疗指南
今天,我们发布了三份针对特定疾病的基因治疗产品开发的新指南。这是FDA为基因治疗产品发布的前三种特定疾病指南。
血友病的人类基因治疗:目前正在开发的血友病基因治疗产品作为单次治疗,可以使患者长期生成体内缺失或异常的凝血因子,减少或消除对凝血因子替代品的需要。为了确定这些产品的正确开发途径,FDA发布了一份《治疗血友病的基因疗法产品的新指南草案(draft guidance on gene therapy products that are targeted to the treatment of hemophilia)》。一旦最终确定,这一新指南将提供关于临床试验设计和临床前考虑因素的建议,以支持这些基因治疗产品的开发。除其他要素外,指南草案还提供了关于替代终点的建议,供加速批准用于治疗血友病的基因治疗产品使用。
视网膜疾病的人类基因治疗:另一个热门领域是治疗视网膜疾病的基因治疗产品。FDA也计划发布《视网膜疾病的人类基因疗法指南( Human Gene Therapy for Retinal Disorders guidance)》。目前在美国进行视网膜疾病临床试验的基因治疗产品通常是玻璃体内注射或视网膜下注射。在一些情况下,基因治疗产品被封装在要植入眼内的装置中。这份新的指南将重点关注视网膜疾病基因治疗的特殊问题,提供了产品开发、临床前测试和临床试验设计相关的建议。
罕见疾病的人类基因治疗:在美国,患病人数少于20万人的疾病被称为罕见病。美国国立卫生研究院报告说,总共近7000种罕见病影响了超过2500万美国人。大约80%的罕见病是由单基因缺陷引起的,大约一半的罕见病都会影响儿童。由于大多数罕见病没有批准的治疗方法,因此存在显著的未满足需求。《罕见病的人类基因疗法指南(Human Gene Therapy for Rare Diseases guidance)》一旦最终确定,将提供关于临床前、制造和临床试验设计的建议。该信息旨在帮助申办者设计临床开发计划,其中可能存在有限的研究人群规模潜在的可行性和安全性问题,以及与解释有效性的问题。
3个基因疗法制造的指南更新
今天,我们还提供了三个现有指南的全面更新,解决了与基因治疗相关的制造问题。
第一份指南,《人类基因治疗研究新药申请(INDs)的化学,制造和控制(CMC)信息》,关于申办方如何提供足够的CMC信息以确保在研基因治疗产品的安全性、均一性、质量、纯度和效力的建议。该指南适用于人类基因疗法,以及含有人类基因疗法的产品与药物或装置组合使用。
第二份指南,《在产品制造和患者随访期间,测试逆转录病毒载体基因治疗产品具有复制能力的逆转录病毒》提供了在制造基于逆转录病毒载体的基因治疗产品期间,以及在接受基于逆转录病毒载体的基因治疗产品的患者的随访监测期间,正确测试RCR的更多建议。具体而言,指南建议确定需要测试的材料和数量。该指南还就一般测试方法提供了建议。
第三份指南,《人类基因治疗产品给药后的长期随访》提供有关设计长期随访(LTFU)观察性研究的建议,以便收集基因治疗产品给药后延迟不良事件的数据。由于基因疗法这样的新技术平台所固有的一些额外不确定性——包括与治疗效果持久性有关的问题,以及基因如果插入不正确,在理论上可能产生脱靶效应——因此,需要在上市后对患者进行重点的长期随访。本指南描述了产品特征、患者相关因素、临床前和临床数据,这些数据在评估长期随访的必要性时应予以考虑,指南还说明了有效的上市后跟踪的特点。
一旦最终确定,这些草案指南将取代FDA在2008年4月(CMC)和2006年11月(RCR和LTFU)发布的更早版本的指南。
基因疗法有望为许多难治性疾病带来高效甚至治愈的希望。其中一些基因产品几乎肯定会改变医疗实践的范式,以及患有某些疾病患者的命运。
FDA的目标是帮助这些创新疗法在确保安全性和有效性的框架内发展,并继续建立人们对这一新兴医学领域的信心。
参考资料:
[1] Statement from FDA Commissioner Scott Gottlieb, M.D. on agency’s efforts to advance development of gene therapies
[2] FDA官网(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发