Cancer Cell重磅发现:经典抑癌基因CDKN2A缺失可促进黑色素瘤转移
| 导读 | Cancer Cell重磅发现:经典抑癌基因CDKN2A缺失可促进黑色素瘤转移。
近日,一项关于黑色素瘤最新成果在线发表于肿瘤研究顶级学术期刊《Cancer Cell》。该研究由美国加州大学旧金山分校黑色素瘤遗传学家Robert Judson领衔,曾汉林博士作为第一作者完成这项工作。
|
近日,一项关于黑色素瘤最新成果在线发表于肿瘤研究顶级学术期刊《Cancer Cell》。该研究由美国加州大学旧金山分校黑色素瘤遗传学家Robert Judson领衔,曾汉林博士作为第一作者完成这项工作【1】。

黑色素瘤是一种由正常黑色素细胞通过逐步累积病理突变最终转化而来的癌症。早期黑色素瘤可以通过手术去除,其五年生存率可达到95%,而一旦黑色素瘤发生侵袭和转移,其五年生存率则骤降到30%以下。因此如何捕捉到黑色素瘤早期侵袭的关键机制则尤为重要。黑色素瘤通常情况下会经历黑痣(nevus),原位黑色素瘤(MIS)到侵袭性黑色素瘤(invasive melanoma),最后发展成远端转移(metastasis)。对于黑色素瘤形成的机制目前还尚并不明确,目前普遍接受的理论是:紫外线照射可刺激黑色素细胞产生BRAFV600E突变,并促使黑色素细胞出现短暂的增殖,随后由于细胞周期抑制基因CDKN2A的基因产物p16INK4A反馈性表达促使细胞进入周期阻滞状态,即痣的形成。而CDKN2A缺失也被认为是黑色素细胞突破痣中细胞周期阻滞状态并最终发展成原位黑色素瘤的关键事件。而这项研究通过分析黑色素瘤病例发现,与经典理论的不一致的是,多数原位黑色素瘤依然表达CDKN2A基因产物,也就是说CDKN2A完全缺失事件并非主要发生在早期原位黑色素瘤阶段,而是集中发生在侵袭性及远端转移性黑色素瘤病人中,这一发现也被同样来自加州大学旧金山分校Boris Bastian教授发表的同期Cancer Cell文章所证实【2】,提示CDKN2A缺失可能参与黑色素瘤早期侵袭和转移。
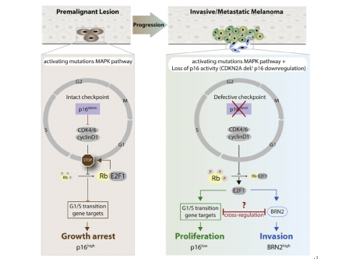
基于此发现,科学家们首先通过CRISPR基因编辑手段对原代黑色素细胞按时序关系逐个引入基因突变,用于更清楚地研究特定突变对健康黑色素细胞的影响,同时,他们通过基因编辑手段能从体外模拟黑色素细胞如何经过一些列有序突变最终转变为黑色素瘤的过程。研究发现,破坏肿瘤抑制基因CDKN2A并不像原先预测的那样简单地帮助肿瘤快速生长,而是同时能促进黑色素细胞的运动和迁移能力,并能在体内促使黑色素瘤发生远端转移。另外,他们还通过进一步机制研究发现,CDKN2A缺失可促进CDK4/6及下游转录因子E2F1激活,并刺激黑色素瘤促转移基因BRN2的表达上调,最终导致肿瘤转移的发生。
作者Robert Judson提出:“这项研究除了确定CDKN2A缺失作为驱动黑色素瘤致命转移能力的关键机制外,这同时还证明了CRISPR基因编辑作为实验室工具研究黑色素瘤及其他肿瘤的新用途。” 同时曾汉林博士也强调:“我们一直以来更多是使用来自晚期癌症的细胞系进行肿瘤研究,但事实上每个细胞的遗传背景差异非常大,这也无疑很难让我们回答到底哪个基因在肿瘤发生发展过程中发生了什么作用,而我们通过对健康细胞进行特定突变,则可以清楚地回答,每个突变到底发挥对肿瘤进展有着什么贡献。”
Highlight from Cancer Cell
另外这项研究同时也为黑色素瘤临床早期诊断提供了新的参考。皮肤科医生目前通过采取可疑皮肤的活检来诊断黑色素瘤。如果病理检测确证为黑色素瘤,病理学家会测量其厚度以进一步确定其进展程度用于判断单纯手术干预是否足以消除肿瘤:黑色素瘤越厚,则判定肿瘤转移的风险越大。但这种方法并不一定可靠,一些薄的黑色素瘤可能已经发生转移,而有些厚的黑色素瘤可能并没有转移。黑色素瘤病理学及基因组学研究先驱Boris Bastian教授强调:“用尺子测量是一个非常粗略的评估肿瘤的进展状态的方法。我们更希望能通过精准检测其遗传突变状态来评估其转变恶性的风险。” CDKN2A缺失促转移的能力的发现也帮助临床医生通过引入CDKN2A缺失等突变作为检测指标更精确地针对黑色素瘤病人进行早期诊断和并找到更合理的治疗方案。

Robert L. Judson: 加州大学旧金山分校皮肤病学系美国加州大学旧金山分校Assistant Researcher, Sandler研究员,NIH DP5 Early Independence Award获得者,及UCSF Helen Diller Family Comprehensive Cancer Center成员。研究方向是基因突变及miRNA/lncRNA参与黑色素瘤发生发展的机制研究。
Hanlin Zeng (曾汉林): 加州大学旧金山分校 UCSF Helen Diller Family Comprehensive Cancer Center博士后研究员,本科毕业于中国药科大学,博士毕业于中国科学院上海药物研究所。研究方向:基因突变对细胞可塑性影响及参与肿瘤转移中的机制研究。
其他作者信息详见文章中作者列表。
Reference
[1] Zeng, H., Jorapur, A., Shain, A.H., Lang, U.E., Torres, R., Zhang, Y., McNeal, A.S., Botton, T., Lin,J., Donne, M., Joseph, N.M., Yeh, I., Bastian, B.C., Judson, L.R. (2018). Bi-allelic loss of CDKN2A initiates melanoma invasion via BRN2 activation. Cancer Cell, Cancer Cell, 34, p56-68.e9.
[2] Shain, A. H., Joseph, N. M., Yu, R., Benhamida J., Liu, S., Prow, T., Ruben, B., North, J., Pincus, L., Yeh, I., Judson, R., Bastian, B. C. (2018). Genomic and Transcriptomic Analysis Reveals Incremental Disruption of Key Signaling Pathways during Melanoma Evolution. Cancer Cell, 34, p45–55.e4.(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发