2018版CSCO肺癌诊疗指南丨在分子分型检测方面说了哪些重点?
| 导读 | 随着肺癌系列致癌驱动基因的相继确定,我国及国际上多项研究表明靶向治疗药物大大改善和延长携带相应驱动基因的非小细胞肺癌(NSCLC) 患者的预后和生存。肺癌的分型也由过去单纯的病理组织学分类,进一步细分为基于驱动基因的分子亚型。 |

基于循证医学证据和精准医学基本原则制定中国常见癌症的诊断和治疗指南,是中国临床肿瘤学会(CSCO) 的基本任务之一。近年来,国际上指南的制定出现了一个新的趋向,即基于资源可及性的指南,这尤其适合发展中国家和地区差异性显著的国家。
中国是一个幅员辽阔但地区发展不平衡的发展中国家,CSCO 指南必须兼顾到地区发展不平衡、药物和治疗措施的可及性以及肿瘤治疗的价值三个方面。因此, CSCO 指南形成了这样的特点,每一个临床问题的诊治指南,分为基本策略和可选策略两部分。基本策略属于可及性好的普适性诊治措施,肿瘤治疗价值相对稳定;可选策略多属于在国际或国内已有高级别证据,但可及性差或效价比超出国人承受能力的药物或治疗措施,如机器人手术。对于一些欧美已批准上市但我国尚不可及的药物,指南专门列出作为临床医生参考。CSCO 指南工作委员会相信,基于资源可及性的指南,是目前最适合我国国情的指南,我们期待大家的反馈并将持续改进,保持 CSCO 指南的时效性。
指南开始阅读之前,先了解下CSCO的证据级别是怎么划分的:
1A 类证据:基于高水平证据(严谨的 Meta 分析或 RCT 结果),专家组有统一共识;
1B 类证据:基于高水平证据(严谨的 Meta 分析或 RCT 结果),专家组有小争议;
2A 类证据:基于低水平证据,专家组有统一认识;
2B 类证据:基于低水平证据,专家组无统一认识,但争议不大;
3 类证据:专家组存在较大争议。
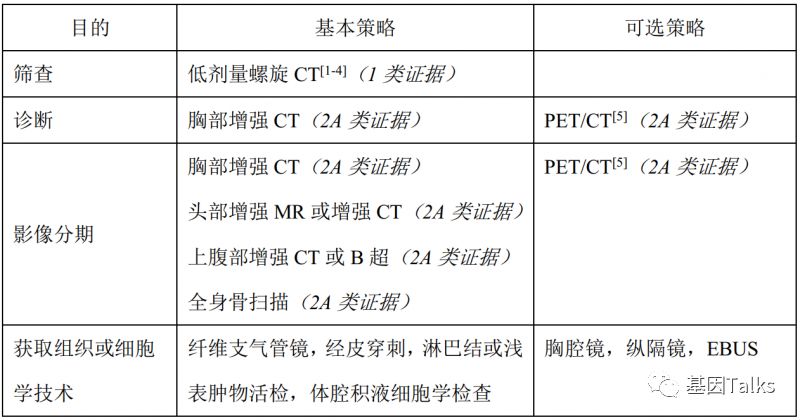
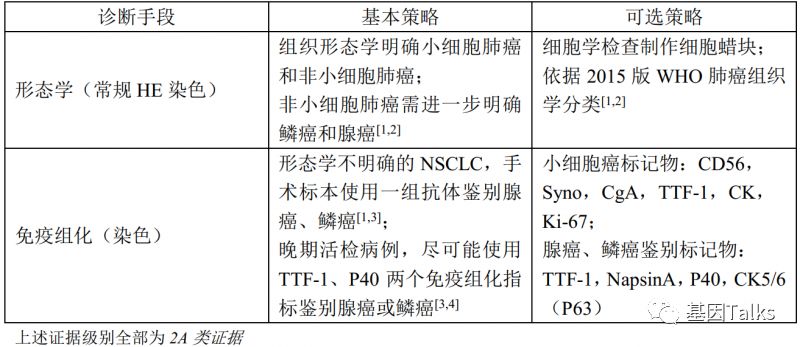
肺癌分为非小细胞肺癌与小细胞肺癌,而大多都为非小细胞肺癌,小细胞肺癌不能通过靶向药治疗,只能通过化疗来治疗,而非小细胞就有很多靶向药可以选择,非小细胞肺癌又分为肺腺癌,肺鳞癌,大细胞癌等。
随着肺癌系列致癌驱动基因的相继确定,我国及国际上多项研究表明靶向治疗药物大大改善和延长携带相应驱动基因的非小细胞肺癌(NSCLC) 患者的预后和生存。肺癌的分型也由过去单纯的病理组织学分类,进一步细分为基于驱动基因的分子亚型。
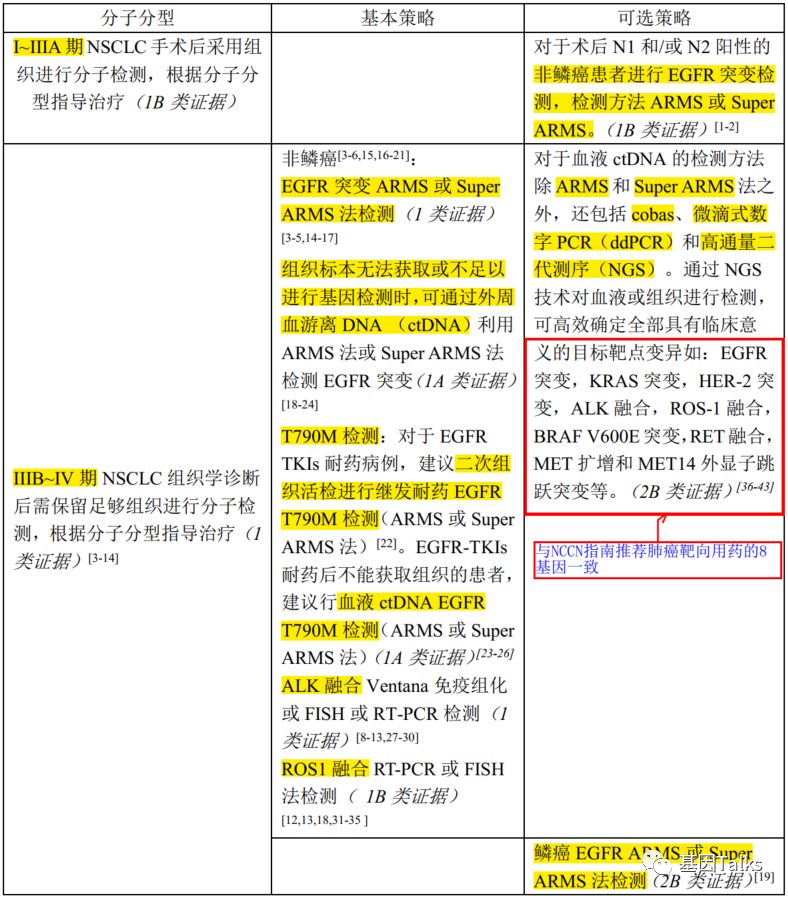
分子分型:(I~IIIA期:可选策略:非鳞癌患者进行EGFR检测;IIIB~IV期:基本策略:非鳞癌患者进行EGFR,ALK,ROS1检测;可选策略:NCCN指南推荐的8基因检测;鳞癌患者进行EGFR检测(2B类证据))
1,晚期表皮生长因子受体(epidermal growth factor receptor, EGFR) 敏感突变和间变性淋巴瘤激酶(anaplasticlymphoma kinase, ALK) 阳性 NSCLC 精准靶向治疗的疗效与分子分型关系已经在临床实践中得到充分证实。今年 Lancet Oncology 发表的重要研究 CTONG1104 以及世界肺癌大会(WCLC)报道的 EVAN 研究结果支持早期术后具有 N1N2的非鳞NSCLC患者进行EGFR突变检测,因术后辅助EGFR酪氨酸激酶抑制剂(EGFR-TKIs)治疗为这部分患者带来了获益。
2. 所有含腺癌成分的 NSCLC,无论其临床特征(如吸烟史,性别,种族,或其他等),应常规进行 EGFR 突变/ ALK 融合基因检测, EGFR 突变检测应涵盖 EGFR 18、 19、 20、 21外显子, ALK 和 ROS1 的检测应与 EGFR 突变检测平行进行。尤其在标本量有限的情况下,可采用经过验证的检测方法同时检测多个驱动基因的技术,如多基因同时检测的 PCR技术或二代测序技术(next generation sequencing, NGS) 等。
3. EGFR 突变/ ALK 融合/ROS1 融合的检测应在患者诊断为晚期 NSCLC 时立即进行,早期肺癌患者演变为Ⅳ期时也应进行 EGFR 突变/ ALK 融合/ROS1 融合的检测。
4. 原发肿瘤和转移灶都适于进行 EGFR 突变/ ALK 融合/ROS1 融合分子检测。
5. 为了避免样本浪费和节约检测时间,对于晚期 NSCLC 活检样本,应根据所选用的技术特点,一次性切出需要诊断组织学类型和进行 EGFR 突变/ ALK融合/ROS1 融合检测的样本量,避免重复切片浪费样本;如果样本不足进行分子检测,建议进行再次取材,确保分子检测有足够样本。
6. 难以获取肿瘤组织样本时,多项回顾性大样本研究显示外周血游离肿瘤 DNA(cell-free tumor DNA, ctDNA)EGFR 基因突变检测相较肿瘤组织检测,具有高度特异性(97.2%~100%)及对 EGFR-TKIs 疗效预测的准确性,但敏感度各家报道不一(50.0%~81.8%)。
欧洲药品管理局 2014 年 9 月已批准当难以获取肿瘤组织样本时,可采用外周血 ctDNA 作为补充标本评估 EGFR 基因突变状态,以明确最可能从吉非替尼治疗中受益的 NSCLC 患者。
CFDA在 2015 年 2 月亦已批准对吉非替尼说明书进行更新,补充了如果肿瘤标本不可评估,则可使用从血液(血浆) 标本中获得的 ctDNA 进行检测,但特别强调 ctDNA EGFR 突变的检测方法必须是已经论证的稳定、可靠且灵敏的方法,以避免出现假阴性和假阳性的结果。
2018年初厦门艾德的 Super-ARMS 试剂盒已经获得中国食品药品管理局(CFDA)的批准, 同时可用于组织及 ctDNA 的基因检测; 其他 ctDNA 的基因检测方法还包括 cobas、微滴式数字 PCR(droplet digital PCR, ddPCR)和 NGS。 因此,当肿瘤组织难以获取时,血液是 EGFR 基因突变检测合适的替代生物标本,也是对可疑组织检测结果的补充。
T790M 突变是一代EGFR-TKI 主要耐药机制之一,占比超过 50%,三代 EGFR-TKI 奥希替尼作用于该靶点,AURA3已证实可有效治疗 EGFR-TKI 治疗进展伴 T790M 突变患者, 奥希替尼在中国已获CSFDA 批准用于 T790M 阳性的一代 EGFR-TKI 耐药患者。 研究报道血浆 ctDNA 可用来检测 T790M 突变,可作为二次活检组织标本不可获取的替代标本,同时也是对可以组织检测结果的补充。
2017 年在 WCLC 会议上报道的前瞻性 BENEFIT 研究, AURA3 研究以及FLAURA 研究的 ctDNA 分析结果再次证明了外周血基础上 EGFR 敏感突变和 T790M 耐药突变检测的可行性。 采用脑脊液、胸腔积液上清等标本进行基因检测目前尚在探索中。
目前对于 ALK/ROS1 融合基因的血液检测,技术尚不成熟,因此对于 ALK/ROS1 融合基因检测,仍该尽最大可能获取组织或细胞学样本进行检测。
7,亚裔人群和我国的肺腺癌患者 EGFR 基因敏感突变阳性率为 40%~50%。 EGFR 突变主要包括 4 种类型:外显子 19 缺失突变、外显子 21 点突变、外显子 18 点突变和外显子20 插入突变。最常见的 EGFR 突变为外显子 19 缺失突变(19DEL) 和外显子 21 点突变(21L858R),均为 EGFR-TKI 的敏感性突变, 18 外显子 G719X、 20 外显子 S768I 和 21 外显子 L861Q 突变亦均为敏感性突变, 20 外显子的 T790M 突变与 EGFR-TKI 获得性耐药有关,还有许多类型的突变临床意义尚不明确。
8. ALK 阳性 NSCLC 的发生率为 3%~7%,东西方人群发生率没有显著差异。中国人群腺癌 ALK 阳性率为 5.1%。而我国 EGFR 和 KRAS 均为野生型的腺癌患者中 ALK 融合基因的阳性率高达 30%~42%。有研究表明,年龄是 ALK 阳性 NSCLC 一项显著的独立预测因子,基于我国人群的研究发现, 在年龄小于 51 岁的年轻患者中, ALK 重排的发生率高达 18.5%;也有研究发现, 在年龄小于 40 岁的年轻患者中, ALK重排的发生率近 20% 。
9. 从检测方法学角度考虑, ALK 阳性 NSCLC 不仅是基因序列层面的改变即序列重排, ALK融合蛋白也是该类疾病中的重要变异。检测技术包括 ALK 基因 FISH 检测、或 ALK 融合变异 RT-PCR 检测、或 ALK 融合蛋白 IHC 检测,该类阳性的肺癌患者通常可从 ALK 抑制剂治疗中获益。
10. 适合 ALK 检测的肿瘤样本,包括肿瘤组织标本和细胞学标本。肿瘤标本获取手段包括手术切除、支气管镜检、经皮肺穿刺、淋巴结活检、手术活检等;对于恶性胸腔积液、心包积液、痰液或支气管灌洗液和细胞学穿刺等样本,恶性胸腔积液等细胞学样本在细胞数量充足条件下可制备细胞学样本蜡块,检测方法可采用 IHC 或 RT-PCR 或 FISH;如果是新鲜细胞标本可考虑采用 RT-PCR 方法。考虑到细胞学样本的细胞数量少等特点,细胞学标本的检测结果解释需格外谨慎。检测实验室应根据组织标本类型选择合适的检测技术。当怀疑一种技术的可靠性时(如 FISH 的肿瘤细胞融合率接近 15%时),可以考虑采用另一种技术加以验证。
11. 目前, CFDA 批准的 ALK 阳性 NSCLC 的诊断试剂盒有雅培贸易(上海) 有限公司的ALK 基因重组检测试剂盒(荧光原位杂交法)、罗氏诊断产品(上海) 有限公司的 Ventana anti-ALK 抗体诊断试剂盒( 免疫组织化学法) 和厦门艾德生物医药科技有限公司的EML4-ALK 融合基因检测试剂盒(荧光 PCR 法)。
12. ROS1 阳性 NSCLC 与 EGFR 突变、 ALK 阳性 NSCLC 一样,是 NSCLC 的另一种特定分子亚型。已有多个研究表明晚期 ROS1 阳性 NSCLC 克唑替尼治疗有效。 CFDA 批准的 ROS1 阳性 NSCLC 的诊断试剂盒为厦门艾德生物医药科技有限公司的 ROS1 融合基因检测试剂盒(荧光 PCR 法)等。
13. 近年,多项研究采用 NGS 针对晚期 NSCLC 进行多基因检测,如目前可作为治疗靶点的基因变异: EGFR 敏感突变, EGFR T790M 突变, KRAS 突变, HER-2 突变, ALK 融合基因, ROS-1 融合基因, BRAF V600E 突变, RET 融合基因, MET 融合基因, MET-14 外显子跳跃突变等。NGS的标本可为组织或外周血游离DNA。NGS的应用提高了临床检测效率,可更加精准的指导 NSCLC 的治疗。同时, NGS 亦可用于发现未知基因,探索动态疗效检测、判断预后及发现耐药机制等。 但目前,由于成本高、检测市场不规范、检测效率和质量不能保证,中国市场仍无足够靶向治疗药物等因素限制了 NGS 的大规模临床应用。
针对 VEGF 通路的小分子酪氨酸激酶抑制剂也在不断研发中, 甲磺酸阿帕替尼和盐酸安罗替尼都是我国自主研发的新药,在阿帕替尼的多中心、随机、安慰剂对照的 II 期临床研究中,135 例二线治疗失败的晚期 NSCLC 患者以 2:1 的比例随机分入阿帕替尼 750mg 组及64安慰剂组,结果显示,ORR 为 12.22% vs 0%(P=0.0158,95%CI 5.46-18.99);PFS 为 4.7个月 vs 1.9 个月(P<0.0001, HR=0.278, 95%CI 0.170-0.455)。阿帕替尼的 III 期研究目前尚在进行中。
2017 年 ASCO 和 WCLC 中发布了盐酸安罗替尼的 III 期临床研究结果(ALTER0303),安罗替尼的靶点除了 VEGFR 之外,还包括 PDGFR、FGFR、 c-Kit 等激酶,研究纳入 437 例至少经两线治疗的 IIIB/IV 期 NSCLC 患者,分别给予安罗替尼(n=294)或安慰剂(n=143),结果显示,安罗替尼单药能够显著延长中位 OS 和 PFS,OS 延长 3.3 个月(9.6 vs 6.3 个月; HR=0.68; 95%CI, 0.54-0.87; p=0.0018),死亡风险下降 32%;PFS 延长 4.0 个月(5.4 vs 1.4 个月; HR=0.25; 95%CI, 0.19-0.31; p<0.0001),亚组分析显示,不论 EGFR 敏感性突变阳性或阴性的患者都能从安罗替尼治疗中获得 PFS 和 OS 获益。
更多关于“盐酸安罗替尼”信息可点击:盐酸安罗替尼丨国产肺癌靶向药,你不了解一下吗?
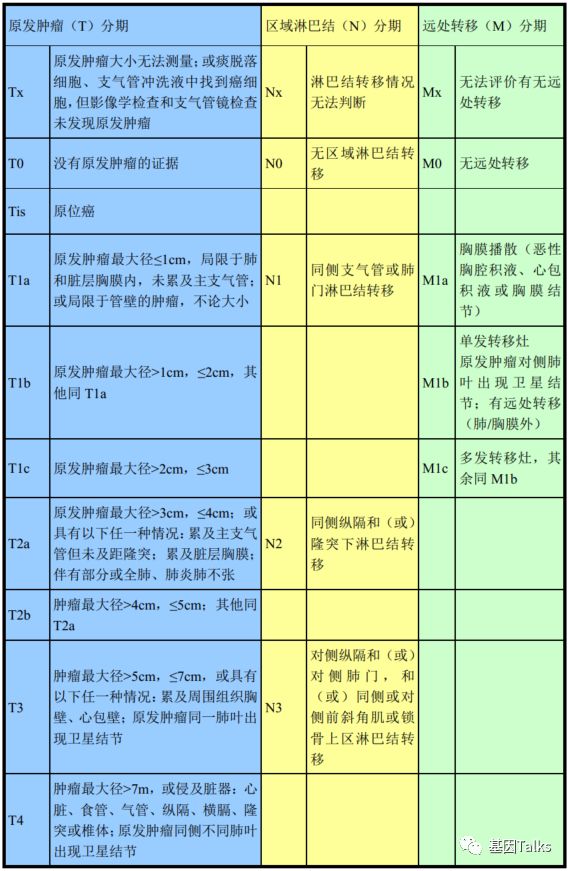
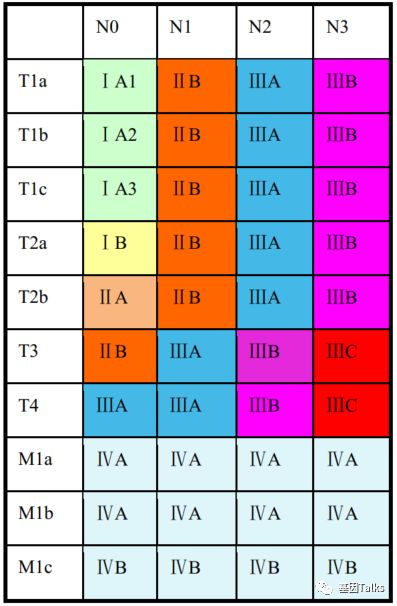
 第 8 版肺癌分期
第 8 版肺癌分期

(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发