最新NEJM和三篇《柳叶刀》公布多项PD1/PDL1抗体联合免疫疗法临床实验结果,治疗多种癌症取得突破性进展!
| 导读 | 饶毅在玩“知识分子”,施一公在做大事!!《Nature》颠覆性突破!革命性颠覆DNA科技或将革了中国首富马云的命!DNA将储存天... |
近日,人类肿瘤里程碑免疫疗法抗PD1抗体联合免疫疗法在临床治疗肿瘤中取得多项突破性进展,结果发表在顶级医学期刊上面。其中顶级学术期刊《新英格兰医学杂志》公布了期待已久的免疫疗法一线治疗肾癌的数据,结果振奋人心,免疫药物组合(Nivolumab + Ipilimumab)在试验中完爆目前的标准疗法-靶向药物Sunitinib;而另一顶级医学期刊《柳叶刀-肿瘤》则发表了三篇与PD1/PDL1相关的肿瘤治疗临床数据,其中一项是也是Nivolumab + Ipilimumab联合治疗黑色素瘤脑转移的2期临床实验数据,另一项则是Nivolumab联合IL-15超级激动剂ALT-803治疗转移性非小细胞肺癌的小型1期临床实验,第三项则是阿斯利康的抗PDL1抗体Durvalumab治疗非小细胞肺癌的2期临床数据。

中国微循环学会转化医学专业委员会成立大会将于2018年7月20日在举世闻名的中国陕西华阴(华山)举行,报名参会的请联系微信7644488。赞助商,媒体合作请联系微信7644488。

肿瘤免疫治疗领域最近真是冰火两重天,一方面因明星免疫疗法IDO抑制剂联合疗法三期临床失败而蒙上巨大阴影;另一方面,人类抗肿瘤史上的里程碑疗法包括抗PD1/PDL1抗体治疗在内的免疫检查点抑制剂治疗以及联合治疗,则一如既往地在多种以往难以对付的肿瘤治疗中取得突破性进展。
近日,人类肿瘤里程碑免疫疗法抗PD1抗体联合免疫疗法在临床治疗肿瘤中取得多项突破性进展,结果发表在顶级医学期刊《新英格兰杂志》以及《柳叶刀-肿瘤》上面。

其中顶级学术期刊《新英格兰医学杂志》公布了期待已久的免疫疗法一线治疗肾癌的数据,结果振奋人心,免疫药物组合(Nivolumab + Ipilimumab)在实验中完爆目前的标准疗法-靶向药物Sunitinib【1】。
而另一顶级医学期刊《柳叶刀-肿瘤》则发表了三篇与PD1/PDL1相关的肿瘤治疗临床数据【2-4】。其中一项是也是Nivolumab + Ipilimumab联合治疗黑色素瘤脑转移的2期临床实验数据;另一项则是Nivolumab联合IL-15超级激动剂ALT-803治疗转移性非小细胞肺癌的小型1期临床实验;第三项则是阿斯利康的抗PDL1抗体Durvalumab治疗非小细胞肺癌的2期临床数据。
▶各种mab分不清◀
目前,免疫检查点抑制剂已经有多种药物被批准上市广泛治疗各种肿瘤,其中,已经有5种抗PD1/PDL1抗体药物上市,包括默沙东的Keytruda、百时美施贵宝的Opdivo、罗氏的Tecentriq、辉瑞和德国默克生产的Bavencio以及阿斯利康生产的Imfinzi。另外,还有一个最早的免疫检查点抑制剂药物,抗CTLA4抗体药物,百时美施贵宝的公司的Yervoy。
这些都是商品名,各种商品名还对应相应的通用名,比如Nivolumab、Ipilimumab等等,而且有些是抗PD1的抗体,有些是抗PDL1的抗体,有时候还真是难以快速分清楚。
因此,我们做了一个表格来帮助读者朋友们以方便大家判断。
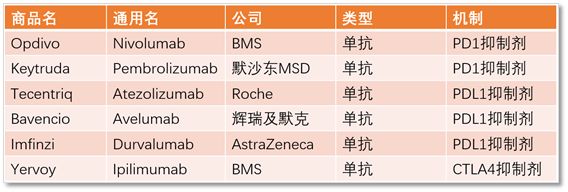
▲目前上市的免疫检查点抑制剂单抗药物相关信息(图片来自转化医学平台)
▶PD1/PDL1与CTLA4机制不同◀
这里既然是要谈《新英格兰杂志》和《柳叶刀》的关于Nivolumab加上Ipilimumab的联合治疗肿瘤的临床试验,就不得不注意一下Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)的不同,本质上还是PD1/PDL1机制与CTLA4机制的不同。
同时使用CTLA4和PD1抑制剂或许是有道理的,因为虽然CTLA4和PD1都表达在T细胞上,它们的抑制机制却不同。CTLA4与CD28竞争性CD80/86信号途径,从而激活T细胞,而PD1则是表达在激活的淋巴细胞上,在耗竭的淋巴细胞上过度表达。看下面这张图就更加明了了,anti-CTLA4抗体作用主要发生在淋巴结中,而anti-PD1/PDL1则主要在肿瘤组织中发挥作用,即发挥作用的位置都不一样。
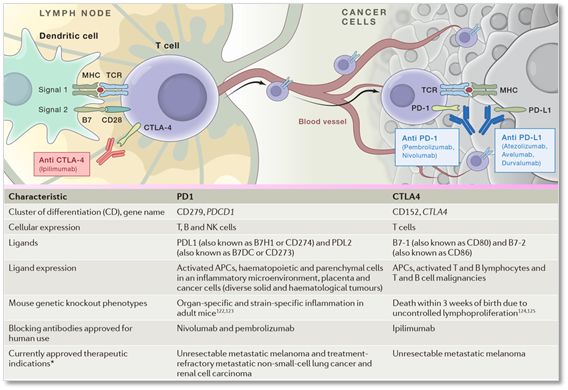
▲尽管都称之为免疫检查点抑制剂,然而,Anti-CTLA4抗体作用主要发生在淋巴结中,而anti-PD1/PDL1则主要在肿瘤组织中发挥作用;这张图罗列了PD1/PDL1与CTLA4的不同之处(图片来自转化医学平台)【5,6】
发挥作用的机制并不完全相同,这就成了Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)联合治疗的基础,否则两个一样的东西用来治疗肿瘤又有什么意义呢?
▶联合治疗完败标准疗法◀
先来看看这篇发表在《新英格兰杂志》上面的超过一千人的大型3期临床实验,题目叫做“Nivolumab plus Ipilimumab versus Sunitinib in Advanced Renal-Cell Carcinoma”,即联合Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)治疗晚期肾细胞癌和最近几年新上市的肾癌标准靶向治疗药物Sunitinib的对比研究。

▲研究者们在《新英格兰杂志》上面发表的文章
晚期肾细胞癌(Advanced Renal-Cell Carcinoma)可以分为低危,中危,高危三种群体,有75%患者都属于中危或高危。
而目前采用靶向治疗药物Sunitinib的标准治疗方法预后也往往不理想。参与这项3期临床研究的肿瘤患者总共有1096人,Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)联合治疗组纳入550人,而单独使用靶向治疗药物Sunitinib组纳入546人。
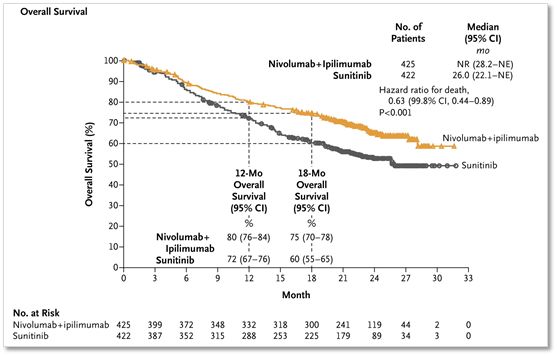
▲Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)联合免疫治疗组的总生存率(黄色线)显著高于单独使用Sunitinib治疗组(黑色线)(图片来自NEJM)
在实验中,联合免疫疗法组肿瘤显著缩小比例高达42%,而标准的靶向药物Sunitinib治疗组只有27%。并且,联合免疫疗法组里面甚至有9%患者监测肿瘤消失。整体来看,免疫疗法的疾病控制率(肿瘤缩小+肿瘤稳定)比例达到了72%。
并且,12个月生存比例,联合免疫疗法组为80%,标准Sunitinib治疗组为72%,18个月的时候,联合免疫疗法组依然有75%,而标准治疗组降到60%。
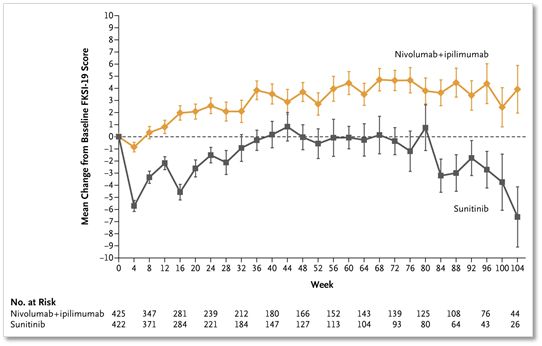
▲Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)联合免疫治疗组患者的生存质量(黄色线)显著高于靶向药物Sunitinib治疗组患者(黑色线)(图片来自NEJM)
更加关键的是,采用国际通用的FKSI-19生活质量调查问卷调查各组治疗的患者之后显示,Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)联合免疫治疗还能够提高患者的生存质量。
▶联合治疗晚期黑色素瘤脑转移◀
而发表在在顶级期刊《柳叶刀-肿瘤》上面的这篇2期临床实验也是联合Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)进行肿瘤治疗,并且,联合治疗组和单独使用Nivolumab(PD1抗体)治疗组的对比研究。
▲研究者们在《柳叶刀-肿瘤》上面发表的文章
研究者们从2014年到2017年间,研究了一种预后非常差的黑色素瘤脑转移的肿瘤患者79人,分成三组,其中A组为Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)联合治疗组(cohort A),纳入36人;B组为Nivolumab单独治疗(cohort B),纳入27人;C组也是Nivolumab单独治疗,但是纳入的患者为常规治疗失败的黑色素瘤脑转移人,16人。
可以这么说,A组和B组的患者的基线状态相似;C组患者病情较重,包括脑部放疗失败、有明显的脑转移症状的患者,甚至包括更凶险的脑膜转移的患者。
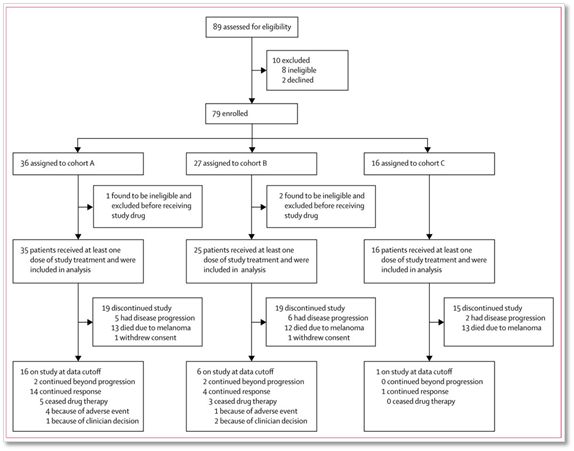
▲患者入组情况(图片来自柳叶刀)
入组情况做好了之后,就开始实验了,A组的36名患者,先使用PD-1抗体Nivolumab(1mg/kg)联合CTLA-4抗体Ipilimumab(3mg/kg)进行治疗,三周一次,进行四次,之后使用Nivolumab单药治疗(3mg/kg,2周一次);而B组和C组患者则使用Nivolumab单药治疗(3mg/kg,2周一次)。
那么,实验结果如何呢?
A组使用联合免疫治疗的36位患者,有16位患者脑部肿瘤明显缩小,颅内有效率高达46%,包括6位(17%)患者脑部肿瘤完全消失;B组使用单药Opdivo的25位患者中,5位患者脑部肿瘤明显缩小,颅内有效率20%,包括3位患者脑部肿瘤完全消失;C组患者状态较差,有效率只有6%。
A组进行联合治疗的患者颅内肿瘤无进展生存期还未达到,6个月生存率78%,而B组单药治疗组患者的颅内肿瘤无进展生存期只有2.5个月,6个月生存率68%。
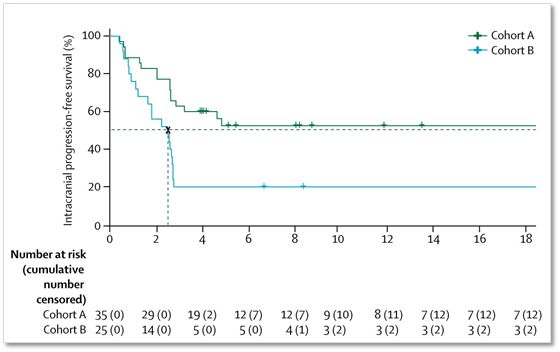
▲A组和B组的颅内肿瘤无进展生存率
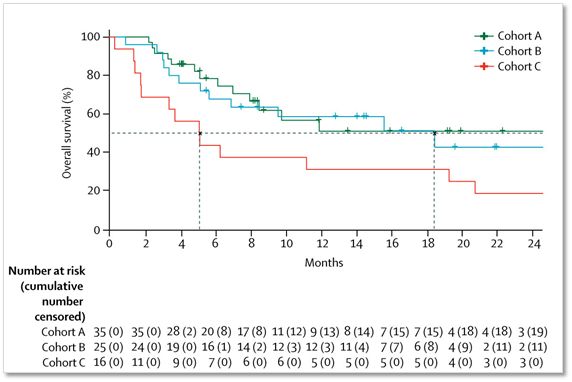
▲各组的总生存率
尽管Nivolumab(PD1抗体)和Ipilimumab(CTLA4抗体)联合治疗组显示出了较好的治疗效果,然而,副作用则相对较大,54%的患者发生3级严重的副作用,9%的患者发生4级严重副作用。相比而言,B组和C组患者的副作用相对较小,分别只有16%和13%的患者发生3级严重的副作用。

▲各组的副作用状况
▶PDL1抗体应用于晚期肺癌◀
接下来这一篇发表在《柳叶刀-肿瘤》上面的2期临床研究评估了阿斯利康的旗舰级药物durvalumab(PD-L1抑制剂)治疗对不同EGFR/ALK和PD-L1肿瘤表达状态的晚期非小细胞肺癌患者的疗效。
▲研究者们在《柳叶刀-肿瘤》上面发表的文章
这项研究自2014年2月25日到2015年12月28日,共纳入444名患者,采用静脉输注Durvalumab治疗(10mg/kg,每2周1次),治疗长达12个月。
该研究根据EGFR/ALK突变状态和肿瘤细胞PD-L1表达情况,将患者分为3组:队列1为:EGFR+/ALK+,即EGFR和ALK阳性,均突变,并且25%以上的肿瘤细胞PD-L1染色阳性;队列2为:EGFR-/ALK-,即EGFR和ALK阴性,均不突变,且25%以上的肿瘤细胞PD-L1染色阳性;队列3为:、EGFR-/ALK-,90%以上的肿瘤细胞PD-L1染色阳性。
研究结果如何呢?
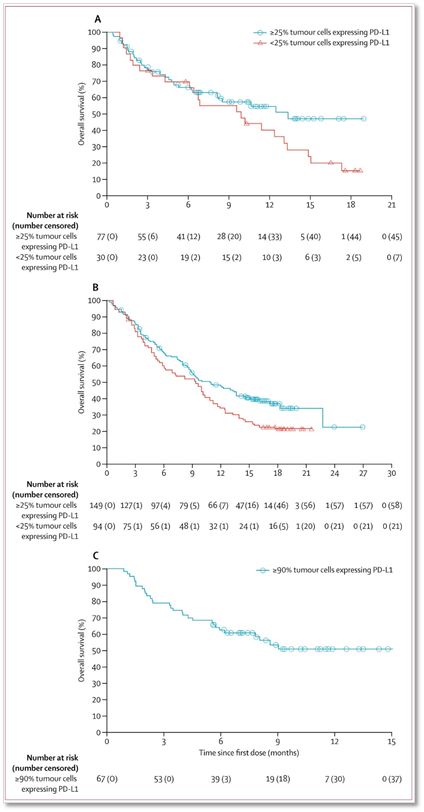
▲各组总生存率
EGFR/ALK阳性患者客观缓解率和中位持续缓解时间劣于EGFR/ALK阴性患者,但中位总生存期和1年生存率并客观缓解率、中位总生存期均优于PD-L1<25%的患者。PD-L1≥90%的EGFR/ALK阴性患者Durvalumab治疗效果最好。
▶强强联合◀
这篇《柳叶刀-肿瘤》文章也是一项关于Nivolumab(PD1抗体)和其他药物联合治疗肿瘤的小型临床实验。
《柳叶刀-肿瘤》还专门为此篇文章配发了题目为“Combining top-ranked immunotherapeutics in lung cancer”的评论文章。
▲研究者们发表的文章
研究者们考察Nivolumab联合IL-15超级激动剂ALT-803治疗转移性非小细胞肺癌的小型1期临床实验,总共纳入23位患者,其中21位接受4个剂量水平的ALT-803联合nivolumab治疗。
ALT-803是一家叫做Altor BioScience的公司开发的一种专有的、新型IL-15“超级激动剂(superagonist)”复合物;在临床前研究中,与IL-15相比,ALT-803具有改善的药代动力学特性和增强的抗肿瘤活性。

而且,研究还表明,针对癌细胞和感染病毒的细胞,ALT-803能同时调动免疫系统的先天免疫和适应性免疫,激发迅速、强大、持久的免疫反应。此外,在各种实验动物模型中,ALT-803也可以有效激活自然杀死细胞(NK cells)和抗体依赖性细胞介导的细胞毒性作用(ADCC)。
而在不久前的2017年5月,美国FDA则授予ALT-803超级激动剂复合物治疗膀胱癌快速通道地位。
那么,为何要选择Nivolumab联合IL-15超级激动剂ALT-803呢?
因为,利用PD-1或PD-L1阻滞的免疫疗法用于未选择的非小细胞肺癌(NSCLC)时,高达80%的患者无反应,而且,其中很多患者在治疗初期会对治疗产生抗药性。而靶向IL-2和IL-15Rβγ共享通路的药物可诱导某些癌症获得完全缓解和持久性反应,然而,目前尚无研究对这些药物与抗PD-1免疫疗法联合治疗的安全性或疗效进行评估。
研究者们将nivolumab采用静脉3mg/kg(后改为240mg)注射方式,14天一疗程(作为新疗法或病程进展期的维持治疗)和IL-15强激动剂ALT-803 皮下用药 1/周(1-5周)6周一疗程,共4个疗程持续6个月。ALT-803的剂量浓度:6、10、15或20ug/kg。
由于1期临床实验主要是考察Nivolumab联合IL-15强激动剂ALT-803的安全性,那么,联合免疫疗法的安全性如何呢?
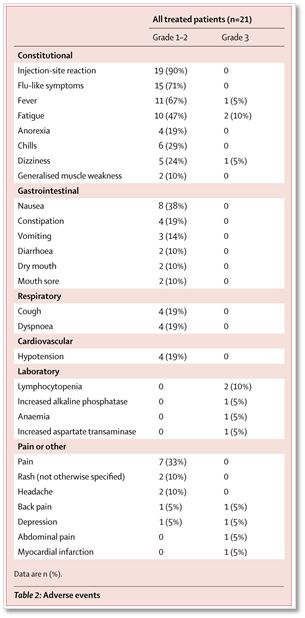
▲Nivolumab联合IL-15强激动剂ALT-803免疫疗法的副作用较低,很少有三级及以上的严重副作用(图片来自柳叶刀)
最常见的副反应是注射点反应(19/21[90%])和流感样症状(15[71%])。其中,有两位患者出现了两种3级副反应:淋巴细胞减少和疲劳,一位患者发生3级心肌梗塞,无4/5级严重副反应。因此,Nivolumab联合IL-15强激动剂ALT-803的安全性还是可以接受的。

参考文献:
1. Nivolumab plus Ipilimumab versusSunitinib in Advanced Renal-Cell Carcinoma
2. Combination nivolumab and ipilimumab ornivolumab alone in melanoma brain metastases: a multicentre randomised phase 2study
3. Durvalumab as third-line or latertreatment for advanced non-small-cell lung cancer (ATLANTIC): an open-label,single-arm, phase 2 study
4. ALT-803, an IL-15 superagonist, incombination with nivolumab in patients with metastatic non-small cell lungcancer: a non-randomised, open-label, phase 1b trial
5. Kathleen M. Mahoney et al. Nat. Rev.Drug. Dis. 2015
6. Gabriel Abril-Rodriguez1 et al. CancerCell. 2017
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发