通过脑室内注射CAR-T首次消灭致命脑瘤的研究团队,这次「盯上」了乳腺癌脑转移
| 导读 | 一项发表在临床领域顶级期刊《新英格兰医学杂志》上的研究表明:先前仅能用来治疗血液肿瘤的 CAR-T疗法在一名胶质母细胞瘤合并脊柱转移患者体内成功消灭了所有的实体肿瘤。而且这是CAR-T疗法首次在实体瘤治疗中获得重大突破! |
1脑室内注射CAR-T细胞首次消灭实体瘤
这项临床试验(NCT02208362)在City of Hope癌症中心进行,所使用的IL13Rα2-CAR T细胞产品(MB-101)是和Mustang Bio公司合作开发的。

接受治疗的是一名50岁的男性患者Richard Grady,他患的是复发性多灶胶质母细胞瘤,在此之前,他接受过肿瘤切除以及化/放疗。患者脑内共有5个肿瘤灶,分别称之为 T1、T2、T3、T4、T5。其中T2、T3在之前接受过不完全切除,而在这次的治疗开始后,它们的附近又出现了两个肿瘤T6、T7。
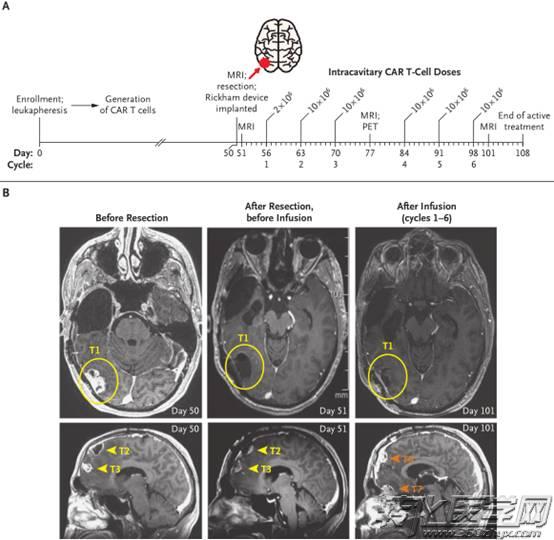
图片来源 NEJM
在此次试验中,患者接受了IL13Rα2-CAR T疗法的治疗,而IL13Rα2这个靶点是首次在CAR-T研究中出现。但更值得注意的是,研究人员采用的是脑室内注射的方法,注射点位于T1附近,第一次的治疗持续了6周时间,肿瘤虽然没有变大,但仍然存在,而T4、T5、T6、T7四个肿瘤灶都有了小幅的增长。同时研究人员发现了患者的肿瘤出现了脊柱转移。
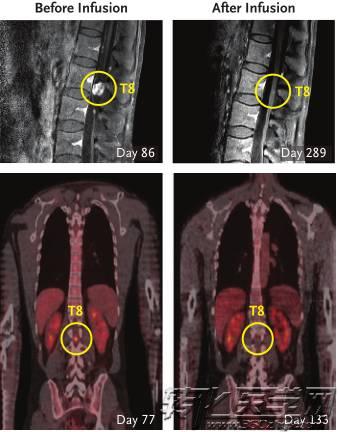
图片来源 NEJM
在第二次治疗中,研究人员在右侧脑室进行了10次注射。注射进行到第3次(第133天)后,患者脑内和脊柱内的所有肿瘤都变小了!在第5次注射(第190天)后,部分肿瘤消失了,剩下一部分减小了77%。在剩下的5次注射结束后,研究人员发现,患者体内的肿瘤全都消失了!在经过严格检查后,在患者体内都没有发现肿瘤的迹象。而且在治疗中几乎没有出现什么严重的副作用。
虽然只是一例患者,但他确实首次让我们知道了CAR-T也许是能突破实体瘤这个底线的。而其中最与众不同的是其CAR-T细胞的给药方式—脑室内注射。
2针对乳腺癌脑转移的CAR-T临床前试验
众所周知,实体瘤相关的肿瘤抗原往往不仅表达于肿瘤组织,在正常组织中亦可有低水平的表达,部分抗原甚至还有维持组织正常生理功能的作用。因此,尽管现行CAR-T细胞治疗采用了阶梯式剂量爬升的输注方式,尽可能减少不良事件的发生,但不良反应仍然存在,其中最为突出的是脱靶效应(on-target off-tumor effects)。
而CAR-T 细胞在非肿瘤组织中接触抗原被激活、增殖,释放大量炎性因子而导致局部脏器的免疫损伤甚至诱发细胞因子风暴,引发严重甚至致死性不良事件。在此之前,曾有HER2 CAR-T细胞回输致死的案例。显而易见,脱靶毒性反应是目前限制CAR-T在实体肿瘤中应用的主要障碍之一。
基于实体瘤所面临的脱靶风险以及脑室内注射首次消灭实体瘤的基础,City Of Hope的研究人员这次“盯上”了乳腺癌脑转移。(乳腺癌作为女性中最常见的恶性肿瘤之一,在世界范围内的发病率仍在逐年上升。其中乳腺癌脑转移的发病率也越来越高。而脑转移癌是影响恶性肿瘤患者生活质量和生存时间的主要因素,同其他部位脏器转移比较,脑转移癌的预后相对较差,总生存期明显缩短。乳腺癌脑转移发生率仅次于肺癌,占脑转移癌第二位,约20%。)
为了避免脱靶风险,他们提出了HER2-CAR T细胞的治疗策略。计划通过两种方式消除这一担忧。在原发性和转移性脑肿瘤部位进行局部或区域性的CAR-T细胞的注射,以绕开大多数表达肿瘤抗原的正常组织,例如HER2。
这项临床前实验,同样是由City Of Hope与Mustam Bio公司共同合作,使用的HER2-CAR T细胞产品为Mustam Bio公司的MB-103. 其是以HER2为靶点的第二代CAR-T疗法,用于治疗乳腺癌脑转移。
美国时间10月31日, Mustam Bio公司公布了MB-103的临床前数据,并在线发表在《Clinical Cancer Research》期刊上。临床前数据表明脑室内直接输注HER2-BBζCAR T细胞能够有效治疗乳腺癌脑转移,支持该疗法的进一步临床试验。

CAR结构(图片来源 aacrjournals.org)
实验设计:在体外实验中,通过测量细胞因子的释放水平,T细胞的增殖数量和肿瘤杀伤能力,比较了含有CD28或4-1BB细胞内共刺激信号转导域的HER2-CAR构建体的功能活性。
在体内实验中,研究人员利用发生乳腺癌脑转移的异种移植物模型,评估了静脉内、局部颅内(local intratumoral)以及区域脑室内(regional intraventricular)三种给药途径对HER2-CART细胞疗效的影响。
实验结果:研究结果显示,与含有CD28共刺激结构域的HER2-CAR相比,含有4-1BB共刺激结构域的HER2-CAR减少了T细胞耗竭表现型,改善了肿瘤靶向性,同时也增强了T细胞的增殖能力。在原位异种移植模型中,HER2-CARs的局部颅内给药显示出了有效的体内抗肿瘤活性。重要的是,研究结果还表明了区域性脑室内注射HER2-CAR T细胞治疗多病灶脑转移和脑膜病变的抗肿瘤效果。
3颅内注射HER2-CAR T细胞有效对抗乳腺癌脑转移
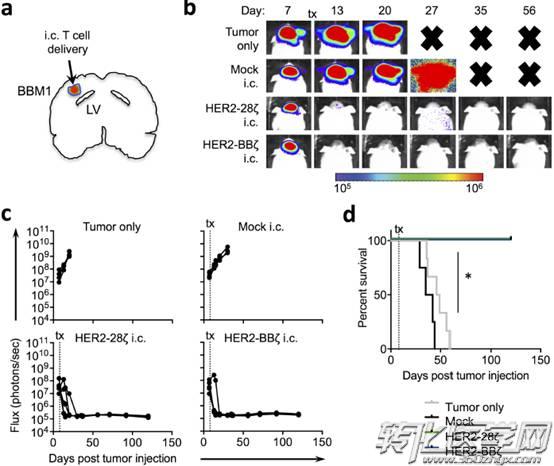
图片来源 aacrjournals.org
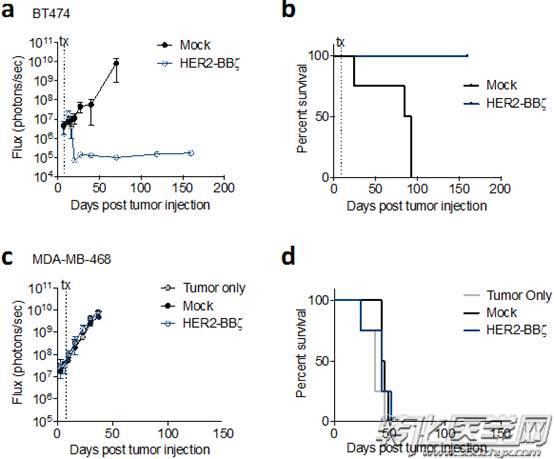
在乳腺癌脑转移的原位移植瘤异种模型中,研究人员通过立体定位注射(stereotactic injection)将HER2-CAR T细胞递送至脑实质。在肿瘤移植后第8天,使用颅内注射(i.c.)将0.5×10^6个HER2-CAR T细胞递送到瘤床(图a),并观察到了肿瘤的完全消退,在第一周时间内,大多数小鼠都产生了抗肿瘤应答(图b和c)。与未处理(仅肿瘤)或Mock(未转导的) T细胞处理的小鼠相比,接受HER2-28ζ和HER2-BBζCAR T细胞治疗的小鼠观察到了相似的反应(生存期延长)(图d)。
以上数据说明了采用颅内注射(i.c.)递送HER2-CAR T细胞可以作为治疗乳腺癌脑转移的有效治疗方法。
4脑室内注射HER2-BBζ CAR T细胞完全消灭乳腺癌脑转移
因为脑转移通常是多病灶的,所以相比较于颅内注射,严格的递送CAR-T细胞可能更受益于区域性。
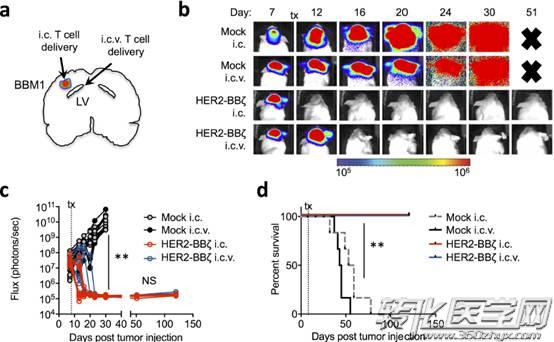
图片来源 aacrjournals.org
在这项临床前试验中,研究人员比较了在BBM1荷瘤小鼠中,区域脑室内注射(regional i.c.v.)和局部颅内注射(local i.c) HER2-CAR T细胞的两种给药途径(图a)。结果观察到等效的抗肿瘤反应(图b和c)和存活时间(图d)。
而相比于局部颅内递送,接受区域脑室内注射HER2-CAR T细胞的小鼠的抗肿瘤反应要稍微延迟一点,这可能是由于需要将这些CAR-T细胞从脑室运送到肿瘤部位。
图片来源 aacrjournals.org
在第14天,研究人员观察到接受脑室内递送的HER2-BBζCAR T细胞治疗的小鼠肿瘤负荷较大。接着,研究人员进一步验证了脑室内注射(i.c.v.)HER2-BBζCAR T细胞在BT474模型(HER2-amplified xenograft model)中的治疗效果(图a和b)。对于三阴乳腺癌异种移植模型(MDA-MB-468),没有观察到抗肿瘤反应(图c和d)。总之,这些临床前研究证明了HER2-CAR T细胞治疗HER2阳性乳腺癌脑转移的疗效。
图片来源 aacrjournals.org
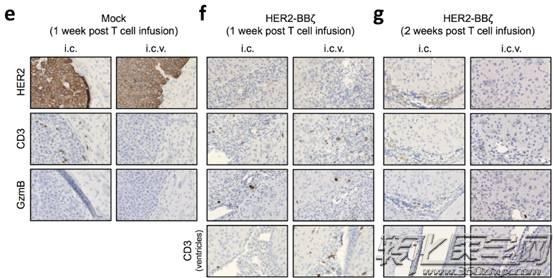
为了评估T细胞的持续性和功能活性,在输注后一周或两周的时间里,研究人员对小鼠组织进行了分析。在局部颅内注射一周后,在肿瘤中发现Mock(未转导)T细胞。接受区域脑室内注射的肿瘤内未发现(图e),但在肿瘤部位都检测到了HER2-BBζCAR T细胞。重要的是,在接受区域脑室内注射(i.c.v)一周后,研究人员在小鼠脑室附近也观察到了T细胞的存在。两周后,尽管数量很少,但T细胞仍然存在(图g)。
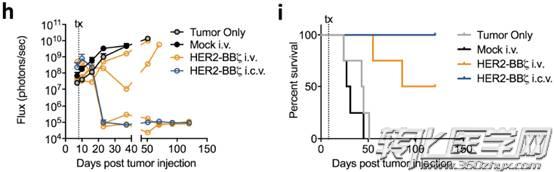
在临床前BBM1模型中,研究人员还比较了区域脑室内注射(i.c.v.)与全身静脉内注射(i.v.)HER2-BBζCAR T细胞对其疗效的影响。
图片来源 aacrjournals.org
区域脑室内注射(i.c.v.)注射HER2-CART细胞(0.5×10^6)显示肿瘤完全消退,而全身静脉内注射(i.v.)递送10倍大剂量HER2-CART细胞(5×10^6)仅显示部分肿瘤消退(图h和i)。有趣的是,研究人员通过流式细胞仪并没有在外周血中观察到HER2-CAR T细胞(i.c.v)。总体而言,这些研究表明在HER2阳性乳腺癌脑转移的临床前模型中,通过区域脑室内注射的HER2-CART细胞具有有效的抗肿瘤疗效。
5脑室内注射HER2-BBζCAR T细胞有效对抗多病灶CNS疾病
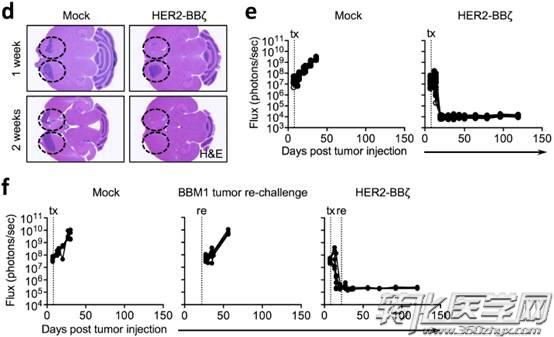
在体内实验中,研究人员针对多病灶CNS病变评估了i.c.v.注射 HER2-CAR T细胞的有效性。为了模拟多病变脑转移,研究人员在小鼠的大脑两半球分别植入了BBM1肿瘤,然后采用脑室内注射HER2-CAR T细胞进行治疗。一周后,一侧的BBM1肿瘤显著缩小。两周后,两侧的肿瘤都完全消除(图d、e和f)。
图片来源 aacrjournals.org
最后,实验数据表明,区域性注射的CAR T细胞可以在肿瘤部位和脑室空间中持续存在至少两周。两周之后,研究人员又进行了肿瘤再复发的实验,发现在不需要额外输注CAR-T细胞的情况下,肿瘤仍能够得到有效控制,并且100%的小鼠存活(数据未显示)。总的来说,该研究小组的临床前模型表明,HER2-BBζCAR-T细胞能够有效消除脑转移性乳腺癌,包括多病灶和柔脑膜HER2 + 中枢神经系统疾病。

Manuel Litchman(图片来源fiercedrugdevforum.com)
对于以上研究结果,Mustang公司的总裁兼首席执行官Manuel Litchman博士表示:“这些令人鼓舞的临床前资料表明,我们的HER2- CAR T细胞疗法对于转移到大脑的HER2 +乳腺癌患者是一种有效的新治疗方案。与此同时,该研究也显示了CAR结构设计在优化CAR-T细胞治疗疗效中的关键,强调了脑室内注射HER2-CAR T细胞可以用于治疗多病灶脑转移和脑膜病变疾病。我们期待着与City Of Hope的研究人员合作继续开展接下来的临床试验 (计划于2018年启动的MB-103的I期临床)。”
参考出处:
http://clincancerres.aacrjournals.org/content/early/2017/10/21/1078-0432.CCR-17-2041#
http://ir.mustangbio.com/News
https://www.statnews.com/2016/12/28/car-t-brain-cancer/
https://clinicaltrials.gov/
http://www.nejm.org/doi/full/10.1056/NEJMoa1610497
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发