液体活检(循环肿瘤细胞)与医学影像学诊断的临床相关性
| 导读 | 摘要:液体活检与医学影像学诊断相互补充和融合,对于肿瘤精准诊疗具有重要临床意义。医学影像学诊断主要包括透视、X线CT、MRI、超声、数字减影、血管造影与PET-CT或SPECT-CT等。液体活检则包含基于筛选和分析血液中完整的循环肿瘤细胞(CTC),由肿瘤细胞释放出的外泌体,和循环肿瘤DNA (ctDNA)等生物标记物,并与下游基因诊断相结合,包括二代测序(NGS),数字PCR等先进的分子诊断技术,推进个性化医疗。 |
摘要:液体活检与医学影像学诊断相互补充和融合,对于肿瘤精准诊疗具有重要临床意义。医学影像学诊断主要包括透视、X线CT、MRI、超声、数字减影、血管造影与PET-CT或SPECT-CT等。液体活检则包含基于筛选和分析血液中完整的循环肿瘤细胞(CTC),由肿瘤细胞释放出的外泌体,和循环肿瘤DNA (ctDNA)等生物标记物,并与下游基因诊断相结合,包括二代测序(NGS),数字PCR等先进的分子诊断技术,推进个性化医疗。
目前影像学合理使用标准是由美国国家综合癌症(NCCN)提供与修订,而NCCN指南被认为是肿瘤治疗的临床策略标准,通常是医学各领域中更新最彻底和最频繁的临床实践指南。自2016年6月至今,已有25份NCCN指南揭示了肿瘤筛查、诊断、分期、治疗效果评估、随访和监测的标准,可与NCCN指南数据库一起离线使用。这些标准包括NCCN指南中所有推荐的影像学程序,NCCN影像学合理应用标准。而液体活检(Liquid biopsy)通过捕获进入到血液的肿瘤细胞或游离DNA,从而替代传统的疾病诊断。已经完成及正在进行的大量研究成果显示在早期肿瘤患者中,利用影像学还未发现病灶时已经可以在外周血中检测到CTC或ctDNA,通过检测CTC的数目可辅助快速评估放化疗及其它治疗手段的疗效,评估肿瘤患者的分期及分级,美国FDA已批准CTC可作为乳腺癌、前列腺癌和结肠癌等肿瘤的独立预后因素,CTC检测数目越高,提示患者预后较差。随着CTC与ctDNA联合检测技术的突破,还可以从血液中收集到活的完整的肿瘤细胞,并对其进行测序,以发现可能导致癌症的突变。这些检测方法可以为更多的患者实现个体化治疗,且每一种新的检测方式都为研究癌症的生物学机制和发病过程提供了一个不同的视角。
相对于影像学、病理学诊断等常规诊断方法,液体活检包括肿瘤的早期筛查,肿瘤标志物检测等在技术成熟度和大数据临床样本积累上还有差距,但是随着液体活检技术的发展与累计,新型诊断技术将逐渐替代原有技术核心,成为肿瘤早筛的首选。液体活检包括肿瘤筛查成为健康人群体检常规项目将指日可待。
1.医学影像学诊断
医学影像学诊断主要包括透视、放射线片、CT、MRI、超声、数字减影、血管造影,心电图仪器、脑电图仪器等,可以作为一种医疗辅助手段用于诊断和治疗,也可以作为一种科研手段用于生命科学的研究中。不仅在临床的应用上非常广泛,对疾病的诊断提供了很大的科学和直观的依据,可以更好的配合临床的症状为最终准确诊断病情起到不可替代的作用。
近30年来,CT、MRI、超声和核素显像设备在不断地改进与完善,检查技术与方法也在不断地创新,影像诊断已从单一依靠形态变化进行诊断发展成为集形态、功能、代谢改变为一体的综合诊断体系。与此同时,一些新的技术如心脏和脑的磁源成像和新的学科分支分子影像学在不断涌现,影像诊断学的范畴仍在不断发展和扩大之中。
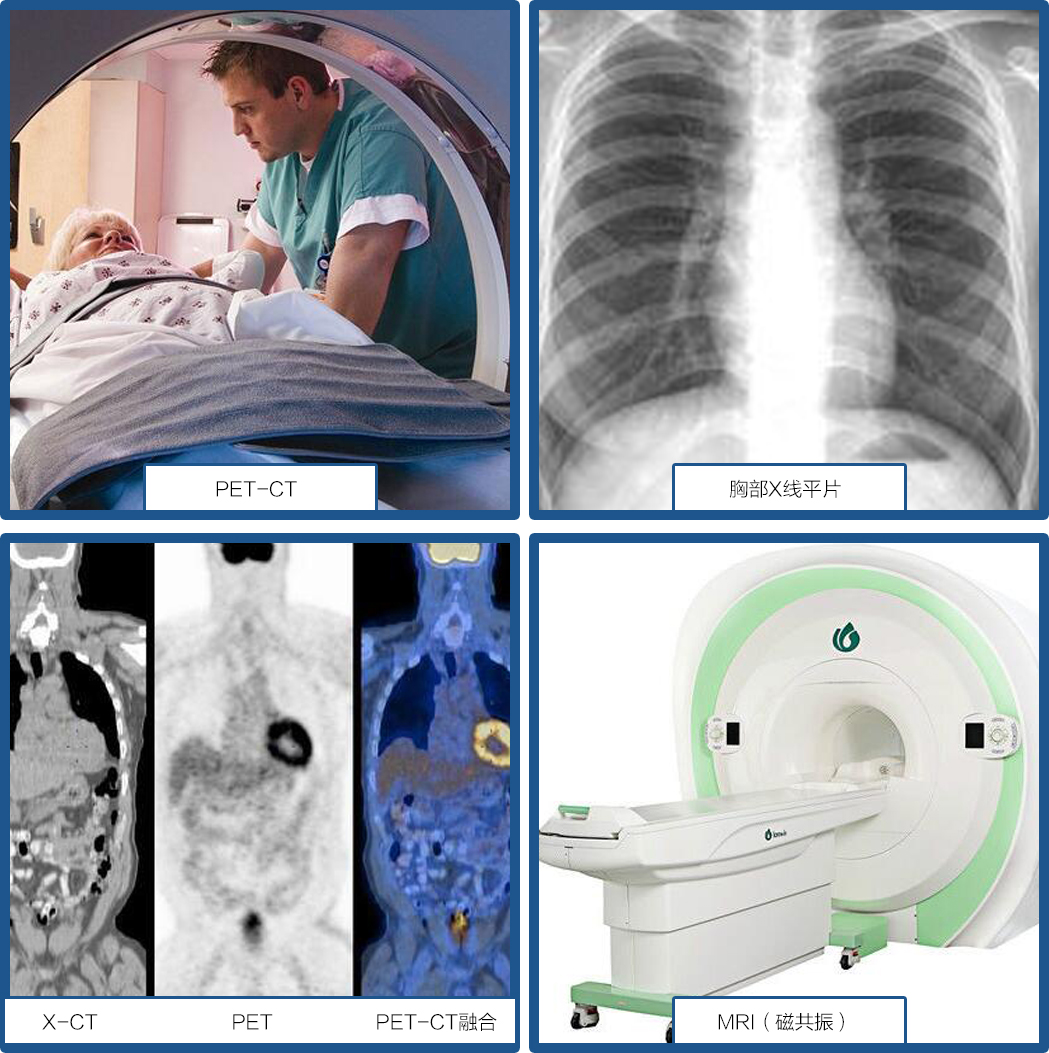
图一:影像学诊断仪器与图片(X-CT,PET-CT)(引用自PET-CT图谱;2011年科学出版社出版与MRI基础;2004年天津翻译出版公司)
1.1 NCCN公布正确的医学影像学使用标准
目前公认的影像学合理使用标准是由美国国家综合癌症网络(NCCN@)与医学诊疗和援助服务中心(CMS)的提供与修订。NCCN持续构建该标准的资料库并面向NCCN肿瘤学临床实践指南(《NCCN指南》发布了《NCCN影像学合理使用标准》。NCCN指南被认为是肿瘤治疗的临床策略标准,通常是医学各领域中更新最彻底和最频繁的临床实践指南。自2016年6月至今,已有25份NCCN指南揭示了NCCN影像学合理使用标准。NCCN影像学合理应用指南是一个易用的、单一来源的关于肿瘤筛查、诊断、分期、治疗效果评估、随访和监测的标准,可与NCCN指南数据库一起离线使用。这些标准包括NCCN指南中所有推荐的影像学程序,包括X线摄片、计算机断层扫描、磁共振成像、功能核医学检查以及超声检查。目前已发布的NCCN影像学合理应用标准面涉及:皮肤基底细胞癌;骨肿瘤;乳腺癌筛查和诊断;中枢神经系统肿瘤;宫颈癌;结直肠癌筛查;隆起性皮肤纤维肉瘤;肾癌;Merkel细胞癌;多发性骨髓瘤;非小细胞肺癌;隐匿性肿瘤(原发不明的肿瘤);皮肤鳞状细胞癌;子宫肿瘤;外阴肿瘤。新的标准可通过一个用户可检索与定制的网络显示界面获取。NCCN影像学合理应用标准全集预计将于2017年发布。
2.液体活检
液体活检(Liquid Biopsy)与传统的组织活检相比有着迅速、便捷、损伤性小等众多优点。临床医生可以用它来监测肿瘤对治疗的反应,预测肿瘤复发,还能够帮助医生在患者未出现任何症状的时候发现最初期的肿瘤。从血液中游离的DNA片段中取得的基因组信息甚至可以指出体内肿瘤发源的部位。研究人员认为,如今的问题已不再是液体活检能否在将来取代手术活检,而是液体活检在何时,以哪种形式取代手术活检。2016年著名的自然杂志《Nature》上发表的一篇文章对不同类型的液体活检进行了归纳总结,文章指出液体活检目前主要有三个方向:分析游离的肿瘤DNA、考察血液中完整的肿瘤细胞(CTC)和收集由肿瘤细胞释放出的外泌体[1]。
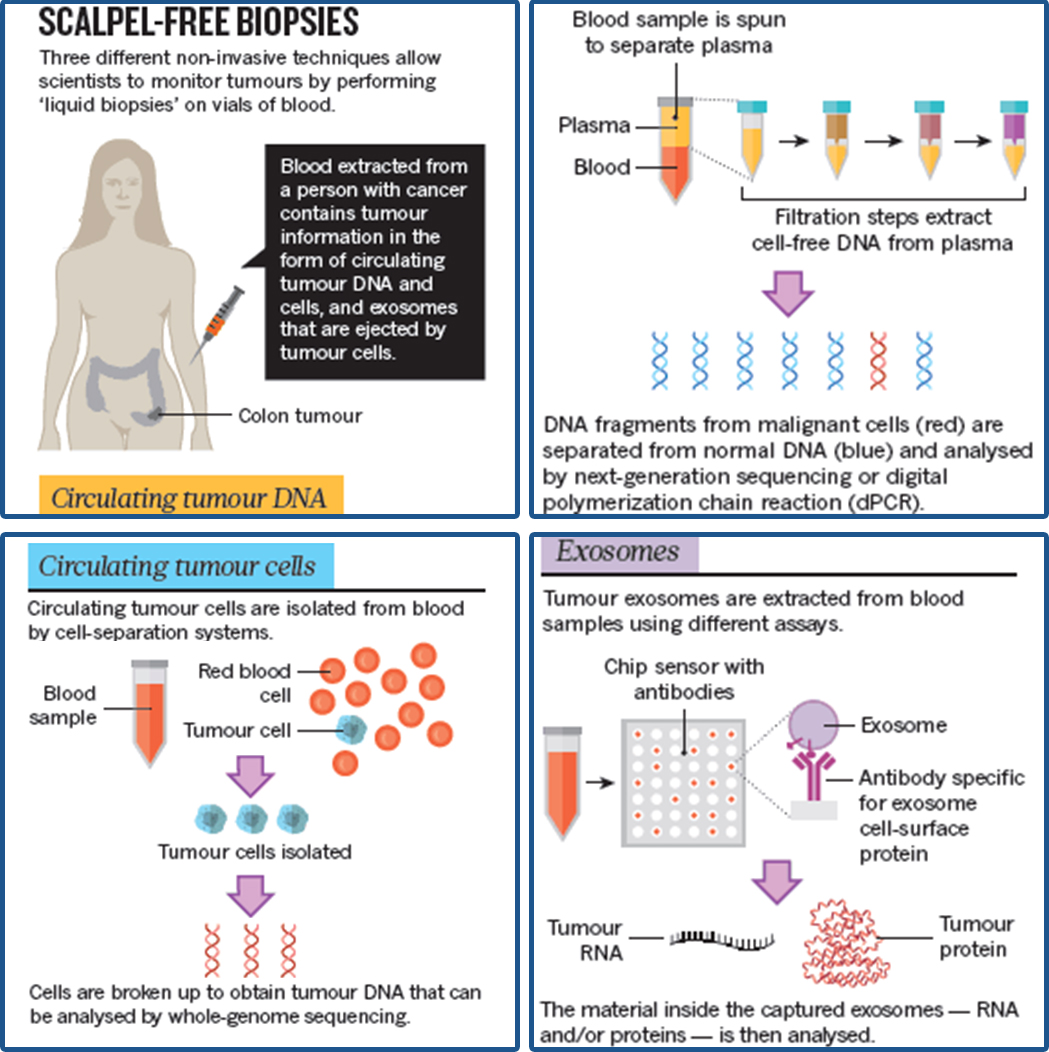
图二:液体活检的种类和方法(引用自Nature. 2016 Apr 14;532(7598):269-71)
2.1 液体活检之一:循环肿瘤细胞
循环肿瘤细胞 (Circulating tumor cell, CTC) 是指从实体瘤中脱离出来并进入外周血液循环的肿瘤细胞。在1896年,澳大利亚学者Ashworth在一例转移性肿瘤患者血液中首次观察到从实体肿瘤中脱离并进入血液循环的肿瘤细胞,并率先提出了CTC的概念。随着CTC临床应用价值凸显,许多研究机构和研发团队都在推出不同的CTC检测技术。目前,CTC检测技术主要分为物理学模式,正向/负向筛选模式或借助微流控芯片(CTC-Chip)。详见美晶医疗转化医学网4月刊的基于微芯片的自动化循环肿瘤细胞检测系统--CellRich™新型液体活检平台。研究发现,在早期肿瘤患者中,利用影像学还未发现病灶时已经可以在外周血中检测到CTC[2]。宁波市第七医院副院长兼外三科主任郝敬铎医师近日在宁波市惠民计划的赞助下,运用美晶医疗的CellRich™新型液体活检平台对转移性结直肠癌患者实施CTC检测时也发现了类似的现象。研究表明,在疾病的早期,外周血循环肿瘤细胞对于良、恶性肿瘤的鉴别有一定的提示价值,也有助于转移风险的预测和判断;在疾病进展和治疗过程中,外周血循环肿瘤细胞能为动态检测病情、耐药性等临床诊疗的关键因素提供重要信息,有助于医师开展个性化的肿瘤治疗。
宁波市医疗中心李惠利东部医院胃肠外科的钱海龙课题组认为循环肿瘤细胞应用于胃癌诊疗中在国内只是刚刚开始,远远没有乳腺癌、结直肠癌等发展得快,因为在我们的认知中胃癌的转移途径是腹腔转移,其CTC数量肯定很少。可是临床结果发现,腹膜转移病人的CTC数量并不少于乳腺癌患者,这就促使我们思考,肿瘤到底是沿血行途径转移还是直接在腹腔内播散的。此外还可以从血液中收集到活的完整的肿瘤细胞,并对其进行测序,以发现可能导致癌症的突变,得以让研究人员通过体外培养或者将它们移植到小鼠体内等方式进行进一步研究。任何从这些实验中获得的知识可以用来指导对病人的治疗。
同院的华永飞主任认为循环肿瘤细胞检测技术的最大好处在于血液标本是比较容易获得的。每次都去寻找肿瘤组织取活检是非常困难的,特别是术后的病人,有创地采集组织风险会很高,况且也不一定就能采到。循环肿瘤细胞至少能帮助我们动态观察了解病人的病情变化,以及监测其发展演变的过程,进而帮助我们及时合理地调整治疗方案,因而具有非常重要的意义。虽然目前仍处于起步阶段,但这项技术在未来的发展前景,即临床的需求及临床的相关性会特别强。
宁波市第二院饶创宙主任认为,目前我们只能对循环肿瘤细胞进行计数,估计患者预后如何:肿瘤细胞数目多,复发转移的几率或许较高,预后欠佳。这些细胞是不是数量多预后就差,对化疗的反应也比较差?我们要知道的是,鉴于循环肿瘤细胞同样具有异质性,它有哪几个类型,属于什么类型,随病人病情的变化发生了什么样的演变,这都是我们想知道的。
2.2 液体活检之二:游离循环肿瘤DNA(ctDNA)
在健康的人体内,每时每刻都有DNA片段流入到血循环中,肿瘤排出的DNA片段也夹杂在其中,而游离循环肿瘤DNA(ctDNA)是由肿瘤细胞释放到血浆中的,携带有与原发肿瘤组织相一致的分子遗传学改变(基因突变)。在临床工作中,肿瘤标志物已经被用来诊断疾病,或者监测治疗效果。但是蛋白类的肿瘤标志物检测容易出现假阳性(或伪阴性),与此相反,ctDNA检测几乎可以排除假阳性结果出现的可能,因为ctDNA的检测结果只是判断受检者是否携带有肿瘤特异性的突变或基因组改变信息。Leon等人的研究结果表明肿瘤患者外周血清DNA水平远高于正常人,之后又在患者的血浆和血清中同时检测到了肿瘤基因突变,并且与原发肿瘤相一致[3]。2013年新英格兰医学杂志的研究结果发现:ctDNA检测作为一种无创的检测方法,能够真实的反映实体瘤组织中的基因突变图谱与频率,是治疗效果的评估及治疗后临床随访的重要监测指标。
2014年Bettegowda[4]和他的同事报道了ctDNA水平在早期和晚期肿瘤(各种癌症)中存在差异。研究人员发现,在640例患者中,ctDNA可检测超过75%的晚期胰腺癌,卵巢癌、结直肠癌、膀胱癌、胃癌、乳腺癌、黑色素瘤、肝癌,以及头颈癌。然而,在原发性脑、肾、前列腺癌和甲状腺癌的检测却不到50%。此外,在206例转移性结直肠癌患者中,源自KRAS基因突变的ctDNA具有87.2%的敏感性和99.2%的异质性。ctDNA作为一种新的肿瘤标志物,将在肿瘤的诊断、治疗及预后检测等方面发挥重要作用,尤其对于一些不具有典型临床症状、检查无特异性和诊断困难的肿瘤可避免复杂的、具有创伤性的活检。ctDNA来自肿瘤细胞的体细胞突变,不同于遗传突变的是,遗传突变存在于体内每个细胞。因此,ctDNA是一种特征性的肿瘤生物标记物,并且还可以被定性、定量和追踪。最近下一代/二代测序技术(NGS)的到来让使用液体活检来分析游离肿瘤DNA成为可能,因为它能够区分肿瘤DNA序列与正常DNA序列。而且,数字PCR(Digital PCR,ddPCR)能够让研究人员量化检测一段特定的肿瘤DNA序列,即使肿瘤DNA的水平只占血液中游离DNA总量的千分之一,这意味着很多液体活检测试将有望被广泛[5]。
2.3 外泌体(EXSOME)
外泌体是活细胞分泌的微小囊泡。这些囊泡中包含了母细胞的DNA、RNA和蛋白。外泌体不但可以从血液中收集,而且可从其他体液(如尿液)中获取。这比从血液中提取更加容易,且更加便捷。最近的研究表明,这些碎片可以作为标记物,来监测疾病的进展,甚至有助于研究人员在症状出现之前诊断癌症。目前,外泌体的研究还处于初级阶段,但是基于外泌体的肿瘤测试已经进入了市场。鲁汶大学人类遗传学中心的Joris Vermeeschzai在European journal of medical genetics杂志发表的一项研究中表明:在大多数的这些肿瘤中,即使是低等级的肿瘤,也可以用一个人的血液,用于研究肿瘤生物学[6]。今年一月,位于马萨诸塞州的生物技术公司Exosome Diagnostics推出的一款基于肿瘤外泌体中RNA检测的血检ExoDx Lung(ALK)成功获得了美国FDA的批准。
2.4 液体活检的临床应用
(1)肿瘤超早期诊断中的应用
体内癌变可分为分子癌变、细胞癌变和组织癌变,ctDNA检测在肿瘤的分子癌变阶段即可实施分子诊断,因此擅长对肿瘤的超早期诊断。而CTC更适用于细胞癌变和组织癌变阶段的诊疗。
(2)判断手术是否成功
ctDNA的浓度与CTC的数量在血液中与肿瘤负荷成正比。在肿瘤手术切除之前,患者血液中的ctDNA浓度或CTC数量较高时,如果肿瘤切除手术成功,术后ctDNA浓度或CTC数量会大幅下降,如果手术不完全成功,术后ctDNA浓度或CTC数量仍保持较高水平,因此根据手术前后血液中ctDNA浓度或CTC数量的变化,可对手术质量进行监测。
(3)监测肿瘤转移复发风险
术后患者血液中ctDNA浓度或CTC数量与肿瘤转移复发风险成正比。如果在术后1-2周,定期检测ctDNA或CTC时发现两者浓度或数量随时间上升,则预示出现肿瘤转移复发的风险上升,如果ctDNA浓度或CTC数量显著下降甚至归零,一般预示转移复发的风险上升较低。
(4)抗癌靶向药物精准使用中的应用
在化疗过程中出现的抗药性一般与肿瘤的基因突变成正比。肿瘤的基因突变会存在于细胞的DNA中。通过检测CTC中的DNA或直接检测血液中的游离DNA,可鉴定出现了哪些新的基因突变。且可根据突变的种类更换适应的靶向胡治疗药物,达到精准医疗的目的。
(5)分析肿瘤异质性中的应用
肿瘤间异质性和肿瘤内异质性一直是困扰临床医师的难题。肿瘤间异质性是指两个同一种癌症患者的肿瘤组织内部分别含有不同的基因突变,肿瘤内异质性是指在一个肿瘤组织内部的不同区域含有不同的基因突变。组织活检很难判断肿瘤异质性,而由于ctDNA或CTC是从肿瘤各个部分凋亡的肿瘤细胞产生的,因此涵盖各种突变,能全面反映肿瘤异质性。
(6)液体活检技术的临床意义
与常规的肿瘤标志物检测,组织切片与医学影像诊断相对比,液体活检(循环肿瘤DNA、CTC与肿瘤来源的外泌体)是基于血液的细胞计数与基因检测,为患者选择更好的治疗方案提供有利条件和证据。液体活检是“更加精准的”的肿瘤标志物。借助于这些更灵敏,更精准的肿瘤标志物,哈佛医学院的Mehmet Toner及其同事分别在2014与2015年的科学杂志上提议[7,8]:“液体活检技术具有巨大的价值。你可以通过液体活检获得完整的细胞,也可以研究DNA、RNA、信号分子、磷酸化模式、遗传学等等,这比单一的生物标志物更加丰富。从长远来看,我们可以培养这些细胞,来测试药物的敏感性,真正走向个性化医学。”
除了DNA和全细胞之外,最近的研究表明,肿瘤细胞脱落的外泌体,也可作为替代的癌症生物标志物。美国德州大学MD安德森癌症中心 Aldape KD以及加拿大多伦多大学Taylor MD带领的一个多国籍多中心的研究小组2014年在《Nature》发表论文,描述了外泌体的一种血清检测法--它携带着DNA、RNA和蛋白质,可以用来成功区分患者早期、晚期胰腺癌与良性胰腺疾病或健康受试者[9]。
尽管液体活检技术取得了巨大的进步并逐渐介入临床辅助诊断,但是液体活检不会取代组织切片或医学影像学诊断,通过血液检测 (也许最终为尿液检测)游离循环DNA或循环肿瘤细胞将在临床工作中扮演重要角色,同时也鼓励通过重复活检为患者选择最佳治疗方案。目前液体活检技术依然面临诸多挑战,例如1:如何寻找更具有特异性的标志物且通过更加先进的技术,进一步提高液体活检检测的灵敏度与特异性;2:液体活检的临床意义需要通过大规模多中心的临床研究予以验证;3:采用通过液体活检技术获得完整的细胞,实施基于CTC致转移复发的遗传机制的研究,探讨CTC作为治疗靶点的临床价值;4:与现有临床检测技术相结合,例如组织切片或医学影像学诊断;5:血液采集系统和分析步骤等的标准化建设。
3. 液体活检与医学影像学检测联合检测的实例与意义
虽然肿瘤的转移过程中癌细胞会基本是通过循环系(血液),从一个器官转移到其他器官,但是不同的癌症转移的器官也不尽相同。比如,乳腺癌更容易转移到肺部,大脑或骨头中,如果可以早期判断出癌细胞转移的方向,那么在症状进一步恶化之前就可以提前采取措施。传统的组织活检,因其局限性,如肿瘤的异质性、肿瘤患者无法进行手术、某些肿瘤解剖位置不便进行穿刺及穿刺自身的临床风险等,可能导致患者无法获得针对性治疗。液体活检作为组织活检的补充,通过非侵入性取样富集血液中的完整肿瘤细胞(CTC),ctDNA或外泌体,可以帮助检测出早期阶段的癌症转移,在动态监测肿瘤进展和治疗反应等领域获得临床认可。尤其这些检测方法是非介入性地,可重复性地抽取肿瘤样本,医生们从而可以建立基因表达谱,靶向突变用药,快速判断治疗是否有效,及随肿瘤的发展而调节治疗方案。
肺癌已成为中国最常见的恶性肿瘤。不少患者因持续咳嗽、咳血及胸痛等临床症状来医院就诊时,通过常规X线胸片检查所发现的肿瘤多数已属中晚期,经手术、放疗、化疗或生物治疗后,5年存活率较低。早期发现诊断、早期治疗是降低肺癌病死率,提高肺癌患者长期生存率的唯一途径。传统检查方法是X线胸片检查,但极易漏诊,主要原因为是1:周围型小肺癌与病灶周边肺组织对比度差;2:正位胸片上,肺组织与纵膈、心脏及膈肌有重叠。且胸部常规螺旋CT检查时的辐射剂量较大,若作为“健康人群”肺癌筛查,不符合放射学检查最优化的原则,因此,液体活检应用于高危人群与高发地区的癌症筛查时,能有助于更精准的发现早期癌症,尤其是亚厘米小结节(直径小于1厘米),将给临床肺部小结节危险分层、临床干预治疗决策提供重要信息参考,从而给广大病人带来巨大福音。
美国密西根综合肿瘤中心Hayes DF教授以及德州大学MD安德森癌症中心Cristofanilli M带领的一个多国籍多中心的研究小组2006年在《肿瘤临床研究》描述了CTC应用于转移性乳腺癌患者放疗前后的预后评估,且与现有影像学诊断相对比[10],研究中纳入了138例患者,其中131例患者实施了1年以上的随访。影像学诊断处于稳定期的患者(S/PR),CTC数量>5个与<5个时,其中位生存期分别是15.3 VS 26.9 个月份,P=0.0389。影像学诊断处于进展期的患者(PD),CTC数量的多少同样与患者生存期呈正相关。CTC数量>5个与<5个的患者其中位生存期分别是 6.4 VS 19.9 个月份,P=0.0039。临床结果显示基线CTC数量的多少与治疗前后CTC数量的增减能预示患者的预后与无进展生存(PFS)及总生存期的长短。通过检测CTC的数目可辅助快速评估放化疗及其它治疗手段的疗效, CTC检测数目越高,提示患者预后较差。相对于现有影像学、病理学诊断等常规诊断方法,在重复取样检测的便利性,诊断结果的前瞻性等方面具有不可取代的优势。随着液体活检技术的发展与累计,新型诊断技术将逐渐替代原有技术核心,成为肿瘤早筛的首选。液体活检包括肿瘤筛查成为健康人群体检常规项目将指日可待。
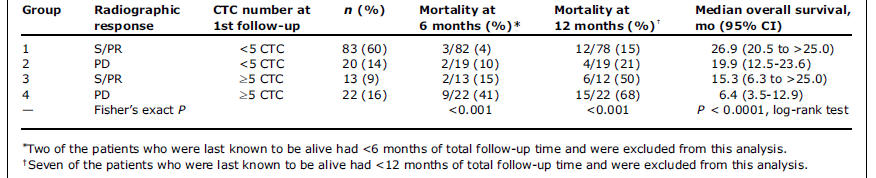
138位转移性乳腺癌患者OS期的影像学与CTC联合解析(引用自Clin Cancer Res. 2006 Nov 1;12(21):6403-9)
4. 液体活检技术平台的国内外现状及展望
CTC,ctDNA 和外泌体虽然都是液态活检的检测对象,但三者的用途不一,必须综合起来才能解决所有问题。比如:CTC 能提高诊疗的精确性,而ctDNA侧重于靶向用药和耐药性指导。外泌体目前还没有成熟的产品,但是外泌体稳定性强,且适用范围广。单一使用CTC 的临床意义将不断降低,CTC的价值将更多展现在与ctDNA 的综合应用,这样可以充分结合ctDNA 高灵敏度,以及CTC 高特异性,全息化的优势。未来,液态活检各种方式的联合使用将是大趋势。
国外的CTC 检测公司大部分都有自己独立研发的检测平台或仪器,例如:Cynveniu 公司的ClearID 微流体平台,Fluxion Biosciences 公司的基于微流体技术以及免疫磁珠的IsoFlux 系统;ApoCell 公司的ApoStream®技术;Clearbridge Biomedics 公司的ClearCell® FX System;Creatv Microtech 公司的CellSieve™微型过滤器。国内的公司具有独立研发的CTC 检测仪器的公司并不多,包括丽珠集团旗下Cynvenio 公司的LiquidBiopsy 稀有细胞分离平台;浚辉生物的植入静脉的CTC 微流控技术GILUPI CellCollector®,博奥晶典的基于微流控的Celsee 系统,宁波美晶医疗的CellRich™循环肿瘤细胞捕获系统等等。(参照宁波美晶医疗官网:
2: Magni E , Zampino MG ,et.al;Detection of circulating tumor cells in patients with locally advanced rectal cancer undergoing neoadjuvant therapy followed by curative surgery;Int J Colorectal Dis. 2014 Sep;29(9):1053-9
3: Leon N , Sommers SC ; Cells of the masculinizing type in ovary of a patient with feminine phenotype;Acta Genet Stat Med. 1967;17(4):345-7
4: Bettegowda C , Diaz LA Jr et al;Detection of circulating tumor DNA in early- and late-stage human malignancies;Sci Transl Med. 2014 Feb 19;6(224)
5: Pécuchet N et al;Base-Position Error Rate Analysis of Next-Generation Sequencing Applied to Circulating Tumor DNA in Non-Small Cell Lung Cancer: A Prospective Study;PLoS Med. 2016 Dec 27;13(12)
6: Vermeesch JR et al;Exome sequencing identifies ZFPM2 as a cause of familial isolated congenital diaphragmatic hernia and possibly cardiovascular malformations;Eur J Med Genet. 2014 May-Jun;57(6):247-52
7: David T. Miyamoto, Mehmet Toner et al;RNA-Seq of Single Prostate CTCs Implicates Noncanonical Wnt Signaling in Antiandrogen Resistance, Science. 2015 September 18; 349(6254): 1351-1356.
8: Aditya Bardia, Mehmet Toner et al;Ex vivo culture of circulating breast tumor cells for individualized testing of drug susceptibility, Science. 2014 July 11; 345(6193): 216-220.
9: Aldape KD ,Taylor MD ,et al;Epigenomic alterations define lethal CIMP-positive ependymomas of infancy. Nature. 2014 Feb 27;506(7489):445-50.
在检验服务方面:满足“精准医疗”对基因检测的需求,设立了美晶医学检验所,已获得卫生部颁发的医疗机构执业许可证书和临床PCR实验室资质。目前美晶医学检验所已开展临床细胞分子遗传学等检验服务,包括个性化用药基因检测,循环肿瘤细胞检测,疾病风险基因检测等多项业务。业务范围覆盖华东,华南地区,已在上海,杭州等地设立了区域营销中心。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发