MMP7
| 导读 | 基质金属蛋白酶(matrix metalloproteinase,MMP)家族是一类依赖金属锌离子的蛋白水解酶家族, 能有效地降解细胞外基质, 在肿瘤的生长、转移过程中均起着重要作用, MMP-7是MMP家族中最小的成员, 可降解各种细胞外基质成分, 如层黏连蛋白、纤维连接蛋白、弹性蛋白、Ⅳ型胶原蛋白等。
国内外的众多研究显示,MMP7启动子区域的多态A-181G能影响MMP7基因的表达,其... |
基质金属蛋白酶(matrix metalloproteinase,MMP)家族是一类依赖金属锌离子的蛋白水解酶家族, 能有效地降解细胞外基质, 在肿瘤的生长、转移过程中均起着重要作用, MMP-7是MMP家族中最小的成员, 可降解各种细胞外基质成分, 如层黏连蛋白、纤维连接蛋白、弹性蛋白、Ⅳ型胶原蛋白等。
国内外的众多研究显示,MMP7启动子区域的多态A-181G能影响MMP7基因的表达,其多态性与卵巢癌、食道癌(ESCC)、非小细胞肺癌(NSCLC)、胃贲门癌(GCA)等多种肿瘤的易感性有关。
基因结构
MMP7全称matrix metallopeptidase 7,基质金属蛋白酶7,位于第11号染色体11q22.3位置。MMP7基因全长10.2kb,mRNA全长1119nt,共有6个外显子,编码由267个氨基酸残基组成的蛋白。
基因分子生物学功能
基质金属蛋白酶(matrix metalloprotinase, MMP)是一类依赖金属锌离子的蛋白水解酶,对细胞外基质(ECM)的降解、组织重建以及细胞内多种可溶性因子的调控起重要作用,是一类与肿瘤发生、侵袭和转移密切相关的蛋白水解酶,与许多恶性肿瘤的发生密切相关。MMP还参与许多生理过程如胚胎发育、血管生成及伤口愈合等。在正常生理状态下,MMP与组织金属蛋白酶抑制剂(tissue inhibitors of metalloproteinases,TIMP)共同调控ECM的更新,维持细胞的稳定性。MMP失调可加速基质屏障的降解,或间接通过释放与基质相关的生长因子来促进肿瘤的生长、侵袭和转移,因此,MMP已成为肿瘤研究和开发抗肿瘤药物的有吸引力的靶点。
大多数MMP酶都作为非活性蛋白被分泌,可以被细胞外的其他蛋白酶裂解后激活。MMP7基因编码的酶降解蛋白聚糖、纤维粘连蛋白、弹性蛋白和酪蛋白。和其他MMP家族酶不同的是,MMP7没有保留蛋白羧基末端区域。
目前的研究发现,MMP-7与卵巢癌、食道癌(ESCC)、非小细胞肺癌(NSCLC)、胃贲门癌(GCA)等多种肿瘤的易感性有关。
参与的通路
Wnt信号通路参与了调控基因表达,细胞发育等重要生理过程,在胚胎发育和肿瘤生长过程中有重要作用。Wnt/β-catenin通路是最经典的Wnt传导通路。此通路的异常激活阻止了β-catenin降解,从而激活了作为关键调控点β-catenin转录活化一系列靶基因,金属基质蛋白酶-7(MMP-7)为其中之一。Wnt通路是一条十分保守的信号传导通路,从低等生物果蝇直至高等哺乳动物,其成员都具有高度的同源性。
目前认为Wnt 通路的组成主要包括:细胞外因子(Wnt)、跨膜受体(frizzled)、胞质蛋白(β-catenin)及核内转录因子(TCF)等一系列蛋白。当细胞外因子与受体结合后,通过一系列胞质蛋白的相互作用使β-catenin蛋白在胞质内累积进而入核与转录因子TCF共同作用激活靶基因的转录。Wnt通路的下游靶基因多数是参与细胞增生与凋亡的基因,如cylinD1、c-myc、MMP7 等。
1. 胞膜上的信号 Wnts是由不同种类的细胞所产生的分泌型糖化蛋白, 通过旁分泌方式发挥作用[1]。Wnt家族至少包含19个富含半胱氨酸的糖化蛋白, 目前仅了解其中的少部分, 例如Wnt-1、Wnt-3a和Wnt-8, 它们激活经典的Wnt/β-catenin途径。Wnt蛋白在胞膜上和一种名为卷曲蛋白 (frizzled, Fz) 的七次跨膜受体相结合, 同时结合辅助受体-低密度脂蛋白受体相关蛋白 (low density lipoprotein receptor related protein LRP-5,LRP-6)。这是Wnt信号通路活化的重要起始信号[2]。Wnt和Fz受体的结合被WIF-1、Cerberus和FzB竞争性抑制, 而Dickkof家族(DKK-1、DKK-2) 通过间接减少可利用的辅助受体LRP的数量来间接抑制Wnt与膜受体的结合[3, 4]。
2. 胞质内的信号 胞质内β-cat的水平在正常情况下被多蛋白降解复合体调控, 这组复合体包括大肠腺瘤息肉蛋白 (APC)、轴蛋白 (Axin)、糖原合成酶激酶 (GSK-3β)和酪蛋白激酶1α/ε(CK1α)。复合体的功能在于使β-cat磷酸化, 而后被泛素-蛋白酶体系统降解。磷酸化的位点在β-cat的N末端结构域, 同时也是肿瘤突变的热点。磷酸化的过程分两步, 第一:丝氨酸残基45被起始CK1α磷酸化。第二:Ser33、Ser37和Thr41被GSK-3β磷酸化[5]。磷酸化后的β-cat被泛素E3连接酶β-TrCP识别从而诱导其泛素化,最终在蛋白酶体里降解。所以正常情况下, 胞质内游离β-cat处于极低的水平。一旦Wnt蛋白与受体Frz结合, 可使胞质内散乱蛋白 (dishevelled,Dsh) 激活,Dsh被磷酸化,Dsh具体的激活机制尚不明了。许多与Dsh相互作用的蛋白, 如Dapper、Frodo、Daam1、PAR-1等已经被识别。它们可以分别和Dsh蛋白不同的部位结合产生激活或抑制Wnt信号的作用[6]。Dsh磷酸化后可以与APC结合, 抑制GSK-3β的活性, 使得β-cat不能被磷酸化[7],引起β-cat在胞质内的积累继而进入胞核。
3.胞核内的信号 积累的β-cat进入胞核与核内转录因子TCF/LEF(T cell factor/lymphoid enhancer factor) 形成复合体, 从而激活一系列Wnt信号靶基因的转录, 包括c-myc、 cyclinD1、MMP-7和免疫球蛋白转录因子2 (ITF-2)。核内β-cat的出现是Wnt信号通路激活的标志。β-cat是Wnt信号通路的正向调节因子, 而APC、 Axin、 GSK-3β等则是负向调节因子。
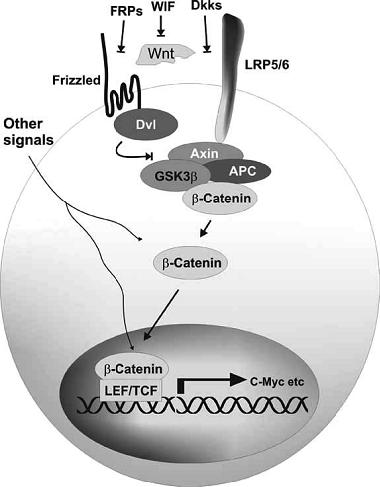
Wnt/β-catenin通路
Wnt/β-catenin通路在肿瘤形成过程中起到关键作用,MMP7是β-catenin/Tcf(T cell factor)的靶点基因之一[8]。研究显示,MMP家族酶的表达受Wnt4通路控制。
基因功能研究
1996年,Knox JD等人[9]定位了MMP7基因在11q21-q22区域。
2000年,Shigemasa等人[10]研究探讨了44例黏液性卵巢肿瘤(良性9例,交界性13例,恶性22例)及6例正常卵巢组织的MMP7的表达,结果所有肿瘤均表达MMP7(p<0.05)。
2003年,Sumi T等人[11]对MMP7与膀胱移形细胞癌(transitional cell carcinoma,TCC)的相关性研究中发现,在20例膀胱TCC病例的样本中,MMP7的表达量在晚期肿瘤细胞中高于初期肿瘤细胞。研究表明,MMP7的表达与晚期膀胱TCC的肿瘤浸润和转移有密切联系。
2003年,Zheng HC等人[12]对MMP7表达和胃癌肿瘤形成﹑发展的相关性研究中发现,在113例胃癌病例中,MMP7在胃癌细胞中的表达明显高于邻近的上皮细胞(P < 0.05)。MMP7的表达与肿瘤大小、Borrmann's分级、入侵深度、转移和TNM状态成正比关系(P < 0.05)。结果显示,MMP7的过表达与肿瘤形成和发展密切相关。
2004年,Surendran K等人 [13]利用大鼠进行的实验表明:MMP家族酶在肾脏管道损伤和管道空隙纤维化过程中起一定作用,在肾脏中,MMP家族酶的表达受Wnt4通路控制。
2006年,胡端敏等人[14]研究了82例胃癌组织及30例周边正常胃黏膜中MMP7的表达情况。结果显示,胃癌组织中MMP7蛋白阳性率显著高于正常胃黏膜(73.2% vs 10%,P<0.001);同时发现MMP-7在TNM分期Ⅲ-Ⅳ期胃癌组阳性率明显高于TNM分期Ⅰ-Ⅱ期胃癌组(P <0.001), 表明MMP-7随胃癌的进展而表达增高;此外有淋巴结转移的胃癌组中阳性率明显高于无淋巴结转移组(P <0.001)。结果表明, MMP-7的表达促使肿瘤细胞向周围组织间隙浸润同时通过淋巴管和血管向远处转移。
国内外的众多研究显示,MMP7启动子区域的多态A-181G能影响MMP7基因的表达,其多态性与卵巢癌、食道癌(ESCC)、非小细胞肺癌(NSCLC)、胃贲门癌(GCA)等多种肿瘤的易感性有关。
基因结构
MMP7全称matrix metallopeptidase 7,基质金属蛋白酶7,位于第11号染色体11q22.3位置。MMP7基因全长10.2kb,mRNA全长1119nt,共有6个外显子,编码由267个氨基酸残基组成的蛋白。
基因分子生物学功能
基质金属蛋白酶(matrix metalloprotinase, MMP)是一类依赖金属锌离子的蛋白水解酶,对细胞外基质(ECM)的降解、组织重建以及细胞内多种可溶性因子的调控起重要作用,是一类与肿瘤发生、侵袭和转移密切相关的蛋白水解酶,与许多恶性肿瘤的发生密切相关。MMP还参与许多生理过程如胚胎发育、血管生成及伤口愈合等。在正常生理状态下,MMP与组织金属蛋白酶抑制剂(tissue inhibitors of metalloproteinases,TIMP)共同调控ECM的更新,维持细胞的稳定性。MMP失调可加速基质屏障的降解,或间接通过释放与基质相关的生长因子来促进肿瘤的生长、侵袭和转移,因此,MMP已成为肿瘤研究和开发抗肿瘤药物的有吸引力的靶点。
大多数MMP酶都作为非活性蛋白被分泌,可以被细胞外的其他蛋白酶裂解后激活。MMP7基因编码的酶降解蛋白聚糖、纤维粘连蛋白、弹性蛋白和酪蛋白。和其他MMP家族酶不同的是,MMP7没有保留蛋白羧基末端区域。
目前的研究发现,MMP-7与卵巢癌、食道癌(ESCC)、非小细胞肺癌(NSCLC)、胃贲门癌(GCA)等多种肿瘤的易感性有关。
参与的通路
Wnt信号通路参与了调控基因表达,细胞发育等重要生理过程,在胚胎发育和肿瘤生长过程中有重要作用。Wnt/β-catenin通路是最经典的Wnt传导通路。此通路的异常激活阻止了β-catenin降解,从而激活了作为关键调控点β-catenin转录活化一系列靶基因,金属基质蛋白酶-7(MMP-7)为其中之一。Wnt通路是一条十分保守的信号传导通路,从低等生物果蝇直至高等哺乳动物,其成员都具有高度的同源性。
目前认为Wnt 通路的组成主要包括:细胞外因子(Wnt)、跨膜受体(frizzled)、胞质蛋白(β-catenin)及核内转录因子(TCF)等一系列蛋白。当细胞外因子与受体结合后,通过一系列胞质蛋白的相互作用使β-catenin蛋白在胞质内累积进而入核与转录因子TCF共同作用激活靶基因的转录。Wnt通路的下游靶基因多数是参与细胞增生与凋亡的基因,如cylinD1、c-myc、MMP7 等。
1. 胞膜上的信号 Wnts是由不同种类的细胞所产生的分泌型糖化蛋白, 通过旁分泌方式发挥作用[1]。Wnt家族至少包含19个富含半胱氨酸的糖化蛋白, 目前仅了解其中的少部分, 例如Wnt-1、Wnt-3a和Wnt-8, 它们激活经典的Wnt/β-catenin途径。Wnt蛋白在胞膜上和一种名为卷曲蛋白 (frizzled, Fz) 的七次跨膜受体相结合, 同时结合辅助受体-低密度脂蛋白受体相关蛋白 (low density lipoprotein receptor related protein LRP-5,LRP-6)。这是Wnt信号通路活化的重要起始信号[2]。Wnt和Fz受体的结合被WIF-1、Cerberus和FzB竞争性抑制, 而Dickkof家族(DKK-1、DKK-2) 通过间接减少可利用的辅助受体LRP的数量来间接抑制Wnt与膜受体的结合[3, 4]。
2. 胞质内的信号 胞质内β-cat的水平在正常情况下被多蛋白降解复合体调控, 这组复合体包括大肠腺瘤息肉蛋白 (APC)、轴蛋白 (Axin)、糖原合成酶激酶 (GSK-3β)和酪蛋白激酶1α/ε(CK1α)。复合体的功能在于使β-cat磷酸化, 而后被泛素-蛋白酶体系统降解。磷酸化的位点在β-cat的N末端结构域, 同时也是肿瘤突变的热点。磷酸化的过程分两步, 第一:丝氨酸残基45被起始CK1α磷酸化。第二:Ser33、Ser37和Thr41被GSK-3β磷酸化[5]。磷酸化后的β-cat被泛素E3连接酶β-TrCP识别从而诱导其泛素化,最终在蛋白酶体里降解。所以正常情况下, 胞质内游离β-cat处于极低的水平。一旦Wnt蛋白与受体Frz结合, 可使胞质内散乱蛋白 (dishevelled,Dsh) 激活,Dsh被磷酸化,Dsh具体的激活机制尚不明了。许多与Dsh相互作用的蛋白, 如Dapper、Frodo、Daam1、PAR-1等已经被识别。它们可以分别和Dsh蛋白不同的部位结合产生激活或抑制Wnt信号的作用[6]。Dsh磷酸化后可以与APC结合, 抑制GSK-3β的活性, 使得β-cat不能被磷酸化[7],引起β-cat在胞质内的积累继而进入胞核。
3.胞核内的信号 积累的β-cat进入胞核与核内转录因子TCF/LEF(T cell factor/lymphoid enhancer factor) 形成复合体, 从而激活一系列Wnt信号靶基因的转录, 包括c-myc、 cyclinD1、MMP-7和免疫球蛋白转录因子2 (ITF-2)。核内β-cat的出现是Wnt信号通路激活的标志。β-cat是Wnt信号通路的正向调节因子, 而APC、 Axin、 GSK-3β等则是负向调节因子。

Wnt/β-catenin通路
Wnt/β-catenin通路在肿瘤形成过程中起到关键作用,MMP7是β-catenin/Tcf(T cell factor)的靶点基因之一[8]。研究显示,MMP家族酶的表达受Wnt4通路控制。
基因功能研究
1996年,Knox JD等人[9]定位了MMP7基因在11q21-q22区域。
2000年,Shigemasa等人[10]研究探讨了44例黏液性卵巢肿瘤(良性9例,交界性13例,恶性22例)及6例正常卵巢组织的MMP7的表达,结果所有肿瘤均表达MMP7(p<0.05)。
2003年,Sumi T等人[11]对MMP7与膀胱移形细胞癌(transitional cell carcinoma,TCC)的相关性研究中发现,在20例膀胱TCC病例的样本中,MMP7的表达量在晚期肿瘤细胞中高于初期肿瘤细胞。研究表明,MMP7的表达与晚期膀胱TCC的肿瘤浸润和转移有密切联系。
2003年,Zheng HC等人[12]对MMP7表达和胃癌肿瘤形成﹑发展的相关性研究中发现,在113例胃癌病例中,MMP7在胃癌细胞中的表达明显高于邻近的上皮细胞(P < 0.05)。MMP7的表达与肿瘤大小、Borrmann's分级、入侵深度、转移和TNM状态成正比关系(P < 0.05)。结果显示,MMP7的过表达与肿瘤形成和发展密切相关。
2004年,Surendran K等人 [13]利用大鼠进行的实验表明:MMP家族酶在肾脏管道损伤和管道空隙纤维化过程中起一定作用,在肾脏中,MMP家族酶的表达受Wnt4通路控制。
2006年,胡端敏等人[14]研究了82例胃癌组织及30例周边正常胃黏膜中MMP7的表达情况。结果显示,胃癌组织中MMP7蛋白阳性率显著高于正常胃黏膜(73.2% vs 10%,P<0.001);同时发现MMP-7在TNM分期Ⅲ-Ⅳ期胃癌组阳性率明显高于TNM分期Ⅰ-Ⅱ期胃癌组(P <0.001), 表明MMP-7随胃癌的进展而表达增高;此外有淋巴结转移的胃癌组中阳性率明显高于无淋巴结转移组(P <0.001)。结果表明, MMP-7的表达促使肿瘤细胞向周围组织间隙浸润同时通过淋巴管和血管向远处转移。
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发