最新高分综述!四川大学华西医院发表:肠道菌群在抗癌治疗中的作用!
| 导读 | 在过去的一段时间里,由于下一代测序技术的快速发展,越来越多的证据阐明了人类微生物群在癌症发展和治疗反应中的复杂作用。更重要的是,现有证据似乎表明,调节肠道微生物群的组成以提高抗癌药物的疗效可能是可行的。然而,存在错综复杂的复杂性,深入了解人类微生物群如何与癌症相互作用对于实现其在癌症治疗中的全部潜力至关重要。 |
5月13日,四川大学华西医院胡建昆教授和杨昆教授在《Signal Transduction and Targeted Therapy》在线发表研究论文“Role of the gut microbiota in anticancer therapy: from molecular mechanisms to clinical applications”,综述了肠道菌群与癌症发展相互作用的分子机制线索,并强调肠道微生物与免疫治疗、化疗、放疗和癌症手术疗效的关系,为制定个体化癌症管理治疗策略提供思路。

https://www.nature.com/articles/s41392-023-01406-7
研究背景
人体微生物群由细菌、真菌、病毒等40种近3000万亿种微生物动态组成,在微生物间表现出不同的丰富度和个体间成分的多样性,对维持系统稳态和功能稳定性具有重要意义。人类微生物群的绝大多数成员位于胃肠道(超过97%),特别是在结肠中,被称为为肠道微生物群,已被广泛研究和证实可介导广泛的生理功能,例如免疫系统的发育和某些营养素的合成。当微生物群和人类宿主之间的平衡受到干扰时,就会发生肠道生态失调,并表现为分类组成、代谢产物和分泌囊泡的变化,所有这些都与包括癌症在内的广泛疾病的生理紊乱有关。
除了消化道内的微生物外,肿瘤内微生物群在精准医学时代也越来越受到关注,因为定植在肿瘤微环境(TME)中的微生物可能是导致癌症进展和患者癌症治疗疗效差异的原因之一。实际上,直到近年来二代和第三代测序的发展,肿瘤内微生物的局部多样性和肿瘤相关意义才得到广泛而深入的研究, 尽管它们的存在早在一个世纪前就被报道过。与其肠道对应物相比,肿瘤内微生物群的复杂表征仍处于婴儿阶段,其作用尚未完全表征,尽管已经对其如何影响肿瘤发生和治疗效果有一些了解。
本文首先总结了肠道和肿瘤微生物致癌作用的分子机制线索,并在此基础上探讨了微生物对常规癌症治疗的意义。此外,还重点介绍了当前和新兴的癌症治疗微生物干预措施及其临床应用,重点是通过微生物策略提高传统癌症治疗效果和减少其副作用的最新主要研究,这可能为制定癌症治疗的个性化治疗策略提供见解。最后,总结了作者对微生物策略在基础研究和临床转化中的展望和挑战的看法。
微生物在肿瘤发生中的机制
促癌细菌可能通过各种不同的分子途径参与肿瘤发生过程,这里总结了四种主要机制:(1)DNA损伤和表观遗传学改变;(2)干扰DNA损伤反应(DDR);(3)异常信号通路;(4)免疫抑制。
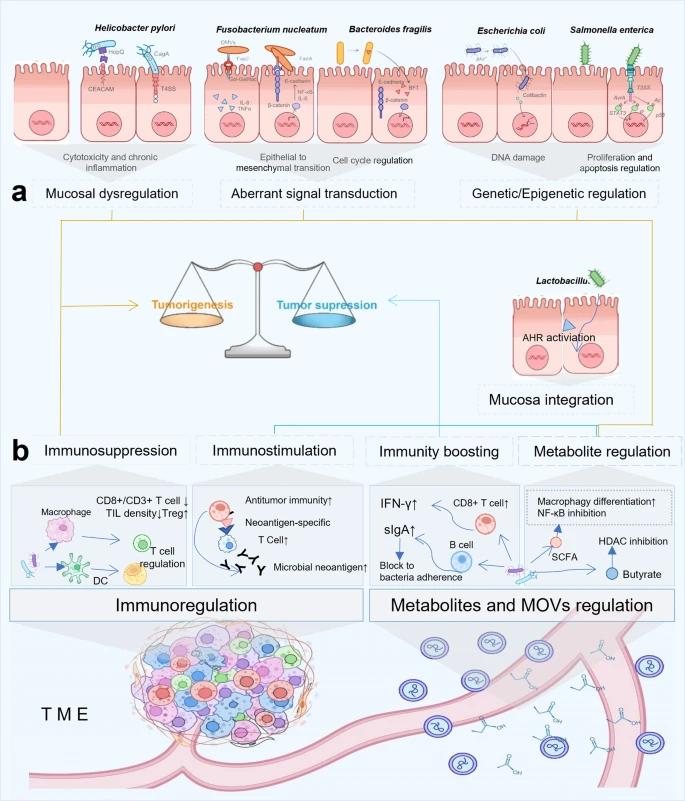
微生物肿瘤发生和肿瘤抑制的机制。
a 微生物在肠道中诱导肿瘤发生和肿瘤抑制的机制:(1)粘膜失调:例如幽门螺杆菌分泌的毒力因子CagA可以通过T4SS与CEACAM和HopQ相结合注入粘膜细胞,从而促进细胞增殖,提高肿瘤细胞的转化率。(2)异常信号转导:例如,从F.nucleatum中提取的Fap2可以通过与Gal-GalNAc结合介导肿瘤进展,来自F.nucleatum的OMV也可以刺激结肠上皮细胞产生TNF并触发IL-8信号传导;FadA是来自F. nucleatum的另一种致病因子,可以与上皮细胞上的E-钙粘蛋白相互作用,并通过Wnt/β-连环蛋白信号激活NF-κB途径,导致肿瘤发生。(3)DNA损伤和诱导遗传/表观遗传学改变:例如肠道沙门氏菌T3SS可以通过基因毒素介导的诱变,结合效应蛋白AvrA和环调节蛋白样蛋白伤寒毒素,在遗传学和表观遗传学上促进肿瘤发生。具体而言,AvrA通过JAK / STAT,Wnt / β-连环蛋白或乙酰转移酶靶向p53途径促进细胞增殖,分化并抑制细胞周期停滞,共同导致肿瘤发生。大肠杆菌可以通过分泌的基因毒素大肠杆菌素诱导DNA损伤,大肠杆菌素可以破坏DNA双链和交联。(4)免疫抑制:例如,肿瘤内微生物可以通过Tregs比例较大、TIL比例较低的PRR连接降低免疫监视效果,例如CD8+T淋巴细胞,从而诱导肿瘤增殖和转移。
b 微生物在TME中诱导肿瘤发生和肿瘤抑制的机制:(1)免疫增强:例如,细菌代谢产物可以提升产生IFN-γ的CD8 + T细胞,增强小鼠模型中ICIs的治疗效果,肠道细菌的SCFAs可以刺激杯状细胞形成粘液,抑制NF-κB活化,引发炎症信号并产生IL-18, 促进B细胞分泌sIgA,从而增强免疫力。(2)代谢物在抗癌活性中的调控:例如,来自共生菌的SCFAs(如丁酸盐)可以诱导巨噬细胞的分化,增加巨噬细胞的抗菌活性,部分是通过抑制HDAC3活性,在糖酵解和自噬中起作用,从而调节肿瘤发生和肿瘤抑制。(CagA细胞毒素相关基因A,T4SS4型分泌系统,CEACAM癌胚抗原相关细胞粘附分子,Hop Q外膜粘附,OMVs外膜囊泡,TNF肿瘤坏死因子,IL-8白细胞介素-8,Treg调节T细胞,TILs肿瘤浸润淋巴细胞,TME肿瘤微环境,IFN-γ干扰素γ,T3SS3型分泌系统,PRR模式识别受体, ICIs免疫检查点抑制剂,sIgA分泌IgA,SCFAs短链脂肪酸,HDAC组蛋白脱乙酰酶)
前景展望
本文综述肠道菌群与癌症发展相互作用的分子机制线索,并强调肠道微生物与免疫治疗、化疗、放疗和癌症手术疗效的关系,为制定个体化癌症管理治疗策略提供思路。此外,还总结了当前和新兴的用于癌症治疗的微生物干预措施及其临床应用。尽管目前仍面临许多挑战,但肠道微生物群对于制定个体化抗癌策略的重要性和全部潜力怎么强调都不为过,有必要探索一种将微生物调节疗法纳入癌症的整体方法。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41392-023-01406-7
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发