【Nature子刊】香港中文大学再发文:揭示“癌细胞”获得“铁死亡”抗性的新途径
| 导读 | 由于缺乏调控铁死亡的关键非编码RNA的研究,本研究旨在揭示参与铁死亡过程的关键非编码RNA。研究人员发现LINC01133可以使胰腺癌细胞对铁死亡更具抗性。 |
近日,香港中文大学研究人员在Nature子刊《Cell Death&Disease》上发表了题为“LINC01133 can induce acquired ferroptosis resistance by enhancing the FSP1 mRNA stability through forming the LINC01133-FUS-FSP1 complex”的研究论文,本研究中,研究人员发现LINC01133高表达与索拉非尼在临床样本中的IC50较高相关。此外,研究人员发现LINC01133通过增强FSP1的mRNA稳定性来诱导这一过程。CEBPB是上调LINC01133表达的转录因子。较高的CEBPB也可能表明索拉非尼在癌症患者中的IC50较高。另外,研究人员证实LINC01133可以与FUS和FSP1形成三重复合体,从而提高FSP1的mRNA稳定性。
https://www.nature.com/articles/s41419-023-06311-z#Sec32
研究背景
01
胰腺癌是一种难治性疾病,其5年预后极差,每年的诊断增长率为0.5 ~ 1%,预计到2030年,胰腺癌将成为所有癌症死亡的第2位。由于缺乏合适的筛查方法,大多数确诊为该病的患者往往处于非常晚期,没有接受手术的机会。虽然一些细胞毒性联合疗法显示出相对较小的获益和严重的副作用,如氟尿嘧啶、亚叶酸、奥沙利铂和伊立替康(FOLFIRINOX),但仍迫切需要更多副作用较轻的辅助治疗替代方案。
细胞死亡过程分为程序性细胞死亡(programmed cell death, PCD)和非程序性细胞死亡(non-programmed cell death, NPCD)两种形式。在PCD中,铁死亡是由Stockwell教授于2012年提出的一种新的PCD模式。此后,越来越多的文献关注这一现象,其潜在的分子机制也逐渐被揭示。主要包括磷脂(PLs)中的多不饱和脂肪酸(PUFA)、铁代谢、抗氧化系统等。许多疾病,如癌症、血色病、心肌病、肝纤维化、缺血再灌注损伤等,已被证实与铁死亡相关。对于某些疾病,如缺血再灌注损伤和肝纤维化,铁死亡似乎参与了疾病的发生发展。而在癌症中,铁死亡已被报道为免疫系统抑制癌症发生和发展的新武器。这表明铁死亡可以被用来对抗传统的化疗不敏感的癌症。尽管铁死亡在改良KPC小鼠中显示出非常有前景的抗肿瘤效果,但获得性铁死亡抵抗仍是可以期待的。
研究结果
02
铁死亡已被证实是一种不同于凋亡的细胞死亡方式,并显示出良好的抗肿瘤作用,特别是在凋亡诱导剂耐药的肿瘤中。有研究表明,在间充质状态的胃癌细胞中,极长链脂肪酸延伸蛋白5 (ELOVL5)和脂肪酸去饱和酶1 (FADS1)表达上调,导致铁死亡增敏,而在肠型胃癌细胞中则相反。在乳腺癌中,二甲双胍联合谷氨酸/胱氨酸反向转运体抑制剂柳氮磺吡啶可促进铁死亡,协同抑制乳腺癌细胞生长。在胰腺癌中,铁死亡诱导剂和凋亡诱导剂的联合应用大大增加了吉西他滨的致死性。尽管铁死亡的机制逐渐被揭示,但与铁死亡相关的关键非编码RNA仍需要更多的探索。在本研究中,研究人员发现LOC105378936, LINC01133, LINC02806, BGIG9606_51662这些尚未被报道与铁死亡相关的基因表现出显著的铁死亡诱导的变化。这些lncrna在三种PAAD细胞系中通过两种不同的铁死亡诱导剂显著增加。综上所述,研究人员发现了一些在铁死亡中发挥作用的关键RNA分子。
lncrna已被证实与癌症的几乎所有标志相关。LINC01133也被报道参与多种癌症的发生发展。前期研究发现LINC01133可通过吸附miR-576-5p抑制胃癌。而在胰腺癌、宫颈癌和肾癌中,前期研究发现LINC01133可以促进其增殖。有趣的是,另一名研究人员发现,LINC01133可以促进胃癌的发展。LINC01133还通过外泌体释放参与上皮-间充质转化。然而,关于LINC01133与铁死亡的研究仍然缺乏。在本研究中,研究人员发现LINC01133可以增加胰腺癌对铁死亡的抵抗。在研究人员建立的铁死亡抵抗的PAAD细胞系中,lncRNA甚至比铁死亡诱导剂处理的组更高。更重要的是,敲低LINC01133可以逆转获得性铁死亡抵抗。较高的LINC01133意味着较高的索拉非尼IC50,这可能在许多癌症中诱导铁死亡。综上,研究人员揭示了癌细胞获得铁死亡抗性的途径,并提供了克服这一过程的方法。
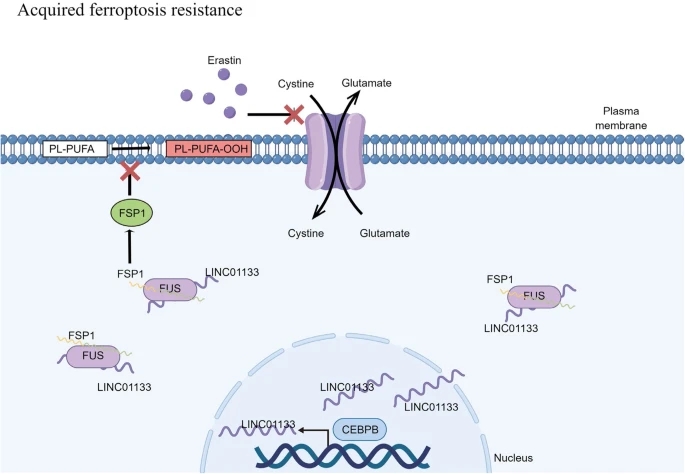
获得铁死亡抗性的机制
研究结论
03
综上所述,研究人员揭示了铁死亡诱导后差异表达的非编码RNA分子。研究人员进一步选择了7个在铁死亡中未被报道的候选物,通过在三个细胞系中使用两种方法诱导铁死亡进行验证。值得注意的是,研究人员进一步证实LINC01133的增加可以降低两种PAAD细胞对铁死亡的敏感性。更重要的是,研究人员建立了耐铁死亡的胰腺癌细胞株,并进一步验证了LINC01133在该细胞株中的功能。LINC01133的降低甚至可以逆转铁死亡抵抗。最后研究人员通过实验验证了LINC01133可以与FUS蛋白和FSP1 mRNA形成三重复合物来增强铁死亡抑制因子FSP1的稳定性,从而降低对铁死亡的敏感性。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41419-023-06311-z#Sec32
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发