神药“二甲双胍”抗癌新机制来了!最新研究:瘤内T细胞缺氧,二甲双胍能救场
| 导读 | 尽管免疫疗法在过去的几十年中在癌症治疗方面取得了革命性的成功,但免疫疗法在某些肿瘤类型和患者中遇到了局限性。 |
近日,由比利时鲁汶大学Benoit J Van den Eynde和Veronica Finisguerra领衔的研究团队,在著名期刊《Journal for ImmunoTherapy of Cancer》发表研究论文“Metformin improves cancer immunotherapy by directly rescuing tumor-infiltrating CD8 T lymphocytes from hypoxia-induced immunosuppression”。研究发现,二甲双胍可以通过减少活性氧产生的方式,将CD8阳性T细胞从缺氧引起的细胞凋亡和免疫抑制中解救出来,增强T细胞的增殖和细胞因子的产生,抑制PD-1和LAG-3表达的上调。重要的是,二甲双胍能在不同的肿瘤模型中增强肿瘤对免疫疗法的反应。

https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10163559/
研究背景
在过去的几年里,免疫疗法已经成为一种非常有前途的癌症治疗方法。免疫疗法的疗效取决于免疫抑制肿瘤微环境中肿瘤抗原特异性CD8 T细胞的活力和功能,其中氧气水平通常较低。缺氧可以通过多种方式降低CD8 T细胞的适应性,CD8 T细胞大多被排除在缺氧肿瘤区域之外。鉴于在临床上实现持久减少缺氧的挑战,改善缺氧条件下的CD8 T细胞存活和效应功能可以改善肿瘤对免疫疗法的反应。
二甲双胍是2型糖尿病的一线疗法,已被证明可以降低糖尿病患者的肿瘤发病率,目前正在几项癌症临床试验中进行评估。据报道,二甲双胍靶向癌症起始干细胞。临床前研究表明二甲双胍与不同类型的免疫疗法之间存在协同作用。二甲双胍可以通过多种机制调节TME,例如,通过减少髓源性抑制细胞(MDSC)的肿瘤内积累或通过减少其抑制表型。二甲双胍也被证明下调PD-L1在癌细胞上的表达,从而改善CD8 T细胞对抗肿瘤的功能。此外,通过线粒体复合物I靶向减少氧化磷酸化,二甲双胍可减轻某些癌症类型的肿瘤缺氧,从而对PD-1阻断,γδ T细胞免疫或放疗产生更好的肿瘤反应。二甲双胍也被证明会影响记忆/效应T细胞分化。特别是,Eikawa等人证明二甲双胍保护肿瘤浸润的CD8 T细胞免于凋亡和衰竭,同时有利于在高度免疫原性的肿瘤模型中从中枢记忆(TCM)到效应记忆T细胞(TEM)的转换。然而,二甲双胍恢复免疫衰竭的细胞和分子机制尚未探索。
研究进展
为了研究缺氧对活化的CD8 T细胞的影响,我们使用了来自TCRP8A转基因小鼠的CD1 T细胞,这些细胞识别MAGE型肿瘤抗原P1A。在常氧中活化4天后,将细胞在21%或1%氧气下孵育24-72小时。与在常氧中孵育的细胞相比,暴露于缺氧会减少细胞数量和扩增;特别是,缺氧增加早期和晚期细胞凋亡,减少CD8 T细胞增殖。有趣的是,当用二甲双胍处理CD8 T细胞时,在1%氧气下孵育的细胞中细胞数量减少和增殖以及诱导细胞凋亡被部分拯救,表明该药物直接改善了CD8 T细胞在缺氧条件下的存活率。OT-1 CD8 T细胞也获得了类似的结果,其识别卵清蛋白抗原肽(OVA)。
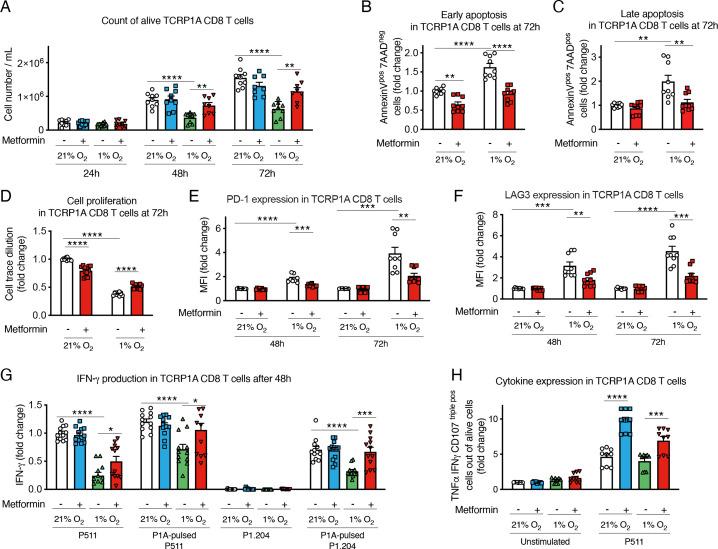
二甲双胍在体外拯救缺氧的CD8 T细胞适应性。
我们还分析了CD8 T细胞表型。如先前报道的,缺氧增加了免疫检查点标志物PD-1和LAG3的表达;然而,二甲双胍减少了这种诱导。与缺氧的免疫抑制作用一致,在低氧张力下孵育可减少与表达P1A抗原(P511)的P815细胞共培养的CD8 T细胞或与P1A抗原肽脉冲的P1A阴性细胞(P1.204)产生干扰素(IFN)-γ;然而,二甲双胍在缺氧条件下响应靶细胞暴露恢复了细胞因子的产生。通过细胞内细胞因子染色(ICS)对肿瘤坏死因子(TNF)-α,IFN-γ和溶酶体相关膜蛋白1(Lamp-1 / CD107)也获得了类似的结果。
这些发现表明,二甲双胍对暴露于缺氧的CD8 T细胞具有直接的有益作用,通过下调耗竭标志物的表达和改善细胞因子的产生,将它们从细胞生长停滞和凋亡中拯救出来,并恢复CD8 T细胞效应功能。
研究意义
在本研究中,我们表明二甲双胍对缺氧、体外和体内的CD8 T细胞存活和适应性有直接影响。这改善了不同肿瘤对免疫疗法的反应,包括我们实验室开发的名为TiRP的本土黑色素瘤模型。该模型表达MAGE型抗原P1A,具有高度免疫抑制性,因此是研究免疫治疗原发性耐药性的临床相关模型。通过这种新描述的作用模式,二甲双胍将CD8 T细胞从限制免疫检查点抑制剂或ACT疗效的强免疫抑制线索中拯救出来。 单独或与淋巴细胞消耗制备药物环磷酰胺(CTX)协同作用,二甲双胍使耐药和缺氧肿瘤对免疫疗法敏感。
这项研究描述了二甲双胍的新作用机制,并提出了一种有希望的策略,可以在缺氧和免疫抑制肿瘤中实现免疫排斥,否则这些肿瘤将对免疫治疗产生耐药性(转化医学网360zhyx.com)。
参考资料:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10163559/
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发